在一定温度下,向体积恒定为2 L的密闭容器中充入2mol M和一定量的N,发生如下反应:M(g)+N(g) E(g)。当反应进行到4 min 时达到平衡,测得M的浓度为0.2 mol/L。下列说法正确的是( )
E(g)。当反应进行到4 min 时达到平衡,测得M的浓度为0.2 mol/L。下列说法正确的是( )
| A.4 min时,E的物质的量浓度为1.6mol/L |
| B.4 min时,用M表示的化学反应速率为0.8mol/(L·min) |
| C.4 min后,向容器中充入不参与反应的稀有气体,M的物质的量减小 |
| D.4 min时,M的转化率为80% |
在Na2SO4、NaCl、NaOH的混合溶液中,含有的Na+、SO42―、OH―个数比是8:1:2,则溶液中Na2SO4、NaCl、NaOH的物质的量之比为()
| A.1:4:2 | B.1:2:4 | C.1:1:1 | D.1:3:2 |
欲配制密度为1.10 g·cm-3、浓度为6 mol·L-1的稀盐酸,在体积为100 mL、密度为1.19 g·cm-3、浓度为12 mol·L-1的浓盐酸中需加蒸馏水()
| A.200 mL | B.100 mL | C.101 mL | D.120 mL |
.实验室分别加热KCIO3、、KMnO4制氧气的反应中电子转移的总数依次是()
| A.12 mol 4 mol | B.6e- 4e- | C.12 e- 4e- | D.6 mol 4 mol |
以下实验装置一般不用于分离物质的是()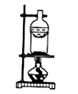

ABC D
体积比为1 : 2 : 3所组成的N2、O2和CO2混合气体100 g在标准状况下体积为()
| A.60 L | B.30 L | C.11.2 L | D.112 L |