下列各选项中所述的两个量,前者一定大于后者的是( )
| A.将pH=4的盐酸和醋酸分别稀释成pH=5的溶液时所加水的量 |
| B.pH=10的NaOH和Na2CO3溶液中水的电离程度 |
| C.相同温度下,10 mL 0.1mol/L的醋酸与100 mL 0.01mol/L的醋酸中H+的物质的量 |
D.物质的量浓度相等的(NH4)2SO4溶液与(NH4)2CO3溶液中NH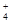 的物质的量浓度 的物质的量浓度 |
常温下,分别将四块形状相同且质量均为7g的铁块同时投入下列四种溶液中,产生气体的速率最快的是
| A.1000mL2mol/LHCl | B.500mL4mol/L H2SO4 |
| C.50ml3mol/LHCl | D.50mL18.4mol/L H2SO4 |
下列说法中正确的是
| A.甲烷分子中只含有非极性键 |
| B.乙烯只能加成、不能取代,苯只能取代、不能加成 |
| C.常温下,苯是一种不溶于水且密度比水小的液体 |
| D.CH3COOH和CH3CH2OH互为同系物 |
A、B、C为三种短周期元素,只有A、B在同一周期,A、C的最低价离子分别为A2-、C--,离子半径A2-大于C-,B2+和C-具有相同的电子层结构。下列判断正确的是
A.原子序数由大到小的顺序是C>A>B
B.原子半径由大到小的顺序是B>A>C
C.离子半径由大到小的顺序是C->B2+>A2-
D.原子最外层电子数由多到少的顺序是B>A>C
下列有关乙烯燃烧的说法不正确的是
| A.点燃乙烯前要先检验乙烯的纯度 |
| B.火焰淡蓝色,产生大量白雾 |
| C.火焰明亮,伴有黑烟 |
| D.120℃时,与足量的氧气在密闭容器中充分燃烧后恢复到原温度,容器内压强不变 |
在粒子NH3D+中,电子数、质子数和中子数之比为:
| A.10:7:11 | B.11:11:8 | C.10:11:8 | D.11: 8:10 |