下列图示与对应的叙述相符的是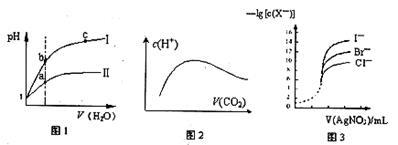
| A.图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.向溶质为1mol的NaOH溶液中通入CO2,随着CO2气体的通入,溶液中水电离出的c(H+)有如上图2变化关系 |
| C.如上图2所示,水电离出c(H+)达到最大值时,溶液中各离子浓度大小分别为 c(Na+)>c(OH-)>c(CO32-)>c(HCO3-)>c(H+) |
| D.用0.0l00mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl- |
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 |
叙述Ⅰ |
叙述Ⅱ |
| A |
NH4Cl为强酸弱碱盐 |
用加热法除去NaCl中的NH4Cl |
| B |
Fe3+具有氧化性 |
用KSCN溶液可以鉴别Fe3+ |
| C |
溶解度:CaCO3<Ca(HCO3)2 |
溶解度:Na2CO3<NaHCO3 |
| D |
SiO2可与HF反应 |
氢氟酸不能保存在玻璃中 |
设nA为阿伏伽德罗常数的数值,下列说法正确的是
| A.常温常压下,8gO2含有2nA个电子 |
| B.1L0.1mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4L盐酸含有nA个HCl分子 |
| D.1molNa与足量氧气反应生成Na2O和Na2O2的混合物,失去nA个电子 |
能在透明溶液中大量共存的一组离子是
| A.Na+、Al3+、Cl-、CO32- | B.H+、Na+、Fe2+、MnO4- |
| C.K+、Cu2+、Cl-、NO3- | D.K+、NH4+、OH-、SO42- |
下列说法正确的是
| A.糖类化合物都具有相同的官能团 | B.酯类物质是形成水果香味的主要成分 |
| C.油脂的皂化反应生成脂肪酸和丙醇 | D.蛋白质的水解产物都含有羧基和羟基 |
固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下: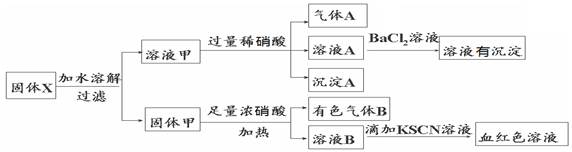
根据上述实验,以下说法正确的是
| A.气体A一定只是NO |
| B.由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液中含有K2SO3 |
| C.若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3 |
| D.溶液甲中一定含有K2SiO3、可能含有KAlO2、MgCl2 |