某溶液中含有NH4+、SO32-、SiO32-、Br一、CO32-、.Na+,向该溶液中通入过量的Cl2,下列判断正确的是
①反应前后,溶液中离子浓度基本保持不变的有NH4+、Na+
②有胶状物质生成
③有气体产生
④溶液颜色发生变化
⑤溶液中共发生了3个氧化还原反应
| A.①⑦③④ | B.①③③④⑤ | C.①③④⑤ | D.②④⑤ |
下列说法中正确的是
| A.8NH3(g)+6NO2(g)===7N2(g)+12H2O(g);ΔH<0,则该反应一定能自发进行 |
| B.提取海带中碘元素时,为将I-完全氧化为I2,用HNO3作氧化剂比用H2O2效果好 |
| C.原电池放电过程中,负极质量一定减轻,正极的质量一定增加 |
| D.由于Ksp(MgCO3)<Ksp[Mg(OH)2],因此水垢中MgCO3会逐渐转化为Mg(OH)2 |
下列表示对应化学反应的离子方程式正确的是
| A.用氨水溶解氯化银沉淀:Ag++2 NH3·H2O=[Ag(NH3)2]++2H2O |
| B.二氧化硫通入氯化铁溶液:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+ |
| C.硫酸氢铵溶液中滴加少量NaOH溶液:H++NH4++2OH-=NH3·H2O+H2O |
| D.碱性条件下铝粉还原NaNO2:NO2-+2Al+3OH-+H2O=2AlO2-+NH3·H2O |
下述实验能达到预期目的的是
| 编号 |
实验内容 |
实验目的 |
| A |
取两只试管,分别加入4 mL 0.01 mol/L KMnO4酸性 溶液,然后向一只试管中加入0.1 mol/L H2C2O4溶液 2 mL,向另一只试管中加入0.1 mol/L H2C2O4溶液 4 mL,记录褪色时间 |
证明草酸浓度越大,反应 速率越快 |
| B |
向含有酚酞的Na2CO3溶液中加入少量BaC12固体, 溶液红色变浅 |
证明Na2CO3溶液中存在 水解平衡 |
| C |
向10mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/L FeCl3溶液,又生成红褐色沉淀 |
证明在相同温度下的Ksp: Mg(OH)2 >Fe(OH)3 |
| D |
测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH, 后者较大 |
证明非金属性S>C |
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,不满足图示转化关系的是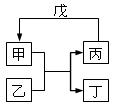
| 甲 |
乙 |
丙 |
戊 |
|
| ① |
NH3 |
O2 |
NO |
H2O |
| ② |
Fe |
H2O |
H2 |
Fe3O4 |
| ③ |
Al2O3 |
NaOH溶液 |
Na AlO2溶液 |
过量CO2 |
| ④ |
Na2O2 |
CO2 |
O2 |
Na |
A.①③ B.②③ C.②④ D.①④
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是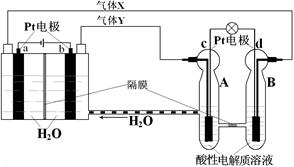
A.转移0.1mol电子时,a电极产生标准状况下O2 1.12L
B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O