下列表示对应化学反应的离子方程式正确的是
A.NaHCO3水解:HCO3- + H2O CO32- + H3O+ CO32- + H3O+ |
B.用石墨作电极电解氯化镁溶液:2Cl- + 2H2O 2OH- + H2↑+ Cl2↑ 2OH- + H2↑+ Cl2↑ |
C.乙醛与新制的Cu(OH)2悬浊液加热:CH3CHO + 2Cu(OH)2 + OH- CH3COO- + Cu2O↓+ 3H2O CH3COO- + Cu2O↓+ 3H2O |
| D.NaAlO2溶液中通入少量二氧化碳:AlO2- + CO2 + 2H2O=Al(OH)3↓+ HCO3- |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g。向另一份中逐渐 加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是()
| A.原混合酸中NO3-物质的量浓度为2 mol/L |
| B.OA段产生的是NO,AB段的反应为 Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是
A.某溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,该溶液pH一定为14-a
B.0.1mol/L的KHA溶液,其pH=10,c(K+)>c(A2-)>c(HA-) >c(OH-)
C.将0.2 mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液: c(HA)>C(Na+)>c(A-)
D.等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:
3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是( )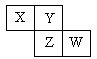
| A.Z元素的原子半径可能比Y元素的小 |
| B.W的原子序数可能是Y的原子序数的2倍 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z的化学活泼性一定比X强 |
分子式为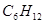 ,分子结构中含有3个“—
,分子结构中含有3个“—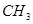 ”原子团的烯烃共有()
”原子团的烯烃共有()
| A.2种 | B.3种 | C.4种 | D.5种 |
下列离子或分子组中能大量共存,且满足相应要求的是()
| 选项 |
离子 |
要求 |
| A |
K+、NO3-、Cl-、HS- |
c(K+)<c(Cl-) |
| B |
Fe3+、NO3-、SO32-、Cl- |
逐滴滴加盐酸立即有气体产生 |
| C |
Na+、HCO3-、Mg2+、SO42- |
逐滴滴加氨水立即有沉淀产生 |
| D |
NH4+、Al3+、SO42-、CH3COOH |
滴加NaOH浓溶液立刻有气体产生 |