下列参数比较及解释均正确的是( )
| 选项 |
参数 |
比较 |
解释 |
| A |
还原性 |
Br->Cl- |
元素的非金属性越强,简单阴离子的还原性越弱 |
| B |
半径 |
Na+<Mg2+<Al3+ |
同一周期粒子半径随原子序数的递增逐渐减小 |
| C |
酸性 |
H2SO3>H2CO3 |
元素的非金属性越强,其含氧酸的酸性越强 |
| D |
沸点 |
HF<HCl<HI |
组成结构相似的物质,相对分子质量越大沸点越高 |
下列有关化学用语表达不正确的是( )
| A.二氧化碳的结构式:O=C=O |
B.S2-的离子结构示意图: |
C.MgO的电子式:[Mg2+][∶ ∶]2- ∶]2- |
D.R2+离子核外有a个电子,b个中子,R原子表示为: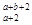 R R |
同周期的X、Y、Z三元素,它们最高价氧化物对应的水化物是HXO4、H2YO4、H3ZO4,则下列判断正确的是( )
| A.含氧酸的酸性H3ZO4>H2YO4>HXO4, |
| B.非金属性X>Y>Z |
| C.元素的负化合价的绝对值按X、Y、Z变小 |
| D.原子半径:X>Y>Z |
下列物质的性质比较,正确的是( )
| A.酸性:H2SO4>HClO4>HBrO4 | B.半径:Li+<Mg2+<Al3+<O2- |
| C.非金属性: P>S>Cl | D.气态氢化物稳定性:HF>HCl>H2S |
下列有关卤族元素的叙述不正确的是()
| A.卤素单质从F2到I2,颜色加深,熔沸点升高 |
| B.卤族元素从Cl到I,最高价氧化物对应水化物的酸性减弱 |
| C.卤族元素从F到I, HX水溶液酸性增强 |
| D.卤素单质氧化性F2>Cl2>Br2>I2,因此排在前面的卤素单质均可将排在后面的卤素从它的盐溶液中置换出来 |
下列有关碱金属元素的叙述正确的是()
| A.碱金属单质均为银白色,密度均小于水 |
| B.碱金属单质从Li到Cs,熔点依次升高 |
| C.氢氧化铯碱性强于氢氧化钠 |
| D.碱金属元素形成的阳离子,从Li+到Cs+氧化性依次增强 |