成熟女性体内有两种促性腺激素:LH(黄体生成素)和 FSH(卵泡刺激素),这两种激素共同参与月经周期的调节,大致的调控机制如图所示。(注:卵泡在排卵后变成黄体)
(1)在排卵前的几天内,雌激素的含量达到第一次高峰,除雌激素外,______的含量也将快速上升,这种调节机制称为______调节,目前市场上购买的排卵试纸就是通过检测这种激素来预测排卵的。
(2)能抑制排卵的激素是________,目前市场上的口服避孕药就是使用这种激素。有一位妇女,口服了含有FSH和LH的药物,这对她的排卵有何影响?______(填“促进排卵”或“抑制排卵”或“几乎无影响”)。
(3)一位妇女因为某一器官受损病变,导致闭经(不排卵,不来月经)。经检查发现她的雌激素含量偏低,但 FSH 和 LH 的含量偏高,据此可判断该妇女受损的器官最可能是______(填“下丘脑”或“垂体”或“卵巢”)。GnRH代表______________激素。
下图为甲病(A、a)和乙病(B、b)的遗传系谱图,其中乙病为伴性遗传病。请回答下列问题:
⑴甲病的致病基因位于染色体上,属于性遗传病;乙病的致病基因位于染色体上,属于性遗传病。
⑵Ⅱ8的基因型为。
⑶假如Ⅱ3和Ⅱ4再生育,生出患甲病孩子的概率是。
图1为DNA分子结构示意图,图2表示细胞内遗传信息表达的过程,请据图回答:
 ⑴图1中,[ ]和[ ]交替连接,构成了DNA分子的基本骨架;⑥的名称是;图中的①②③是否构成了胞嘧啶脱氧核苷酸(填“是”或“否”)。
⑴图1中,[ ]和[ ]交替连接,构成了DNA分子的基本骨架;⑥的名称是;图中的①②③是否构成了胞嘧啶脱氧核苷酸(填“是”或“否”)。
⑵图2中,②的名称是,④的名称是。
⑶假设图2的①中共有600个碱基对,则由它控制形成的②中含有个密码子,最多需要个④来搬运氨基酸,最终合成的蛋白质中氨基酸最多不超过种。
⑷请据图2中的②链写出①中模板链的相应的碱基排列顺序:,写出与②对应的⑤中氨基酸的排列顺序:。
(密码子表:酪氨酸:UAC;甲硫氨酸:AUG;丙氨酸:GCU;精氨酸:CGA;
丝氨酸:UCU;异亮氨酸:AUU;终止:UAA)
⑸根据图2请用文字和箭头表示出该细胞内遗传信息表达的过程:。
R型肺炎双球菌菌体无多糖类的荚膜,是无毒性细菌;S型肺炎双球菌菌体有多糖类的荚膜,是有毒性细菌,使人患肺炎或使小鼠患败血症。科学家艾弗里及其同事利用肺炎双球菌来探究什么是遗传物质的问题。
实验材料、用具:S型细菌、DNA水解酶、培养基、培养器等。艾弗里等人先做了三组实验:
①S型细菌的蛋白质+R型活细菌R型菌落
②S型细菌荚膜的多糖+R型活细菌R型菌落
③S型细菌的DNA+R型活细菌R+S型菌落
(1)艾里弗等人后来发现上述实验步骤并不严密,于是又做了第四组实验,请按照
①②③中表达式写出第四组实验方法和结果:
④_____________________________________________________。
(2)从上述实验可以得出结论__________________________________________。
(3)从③④组实验可知,S型细菌的DNA或基因能否通过R型细菌的细胞膜?____。
(4)有人认为,上述四组实验并不能说明蛋白质和多糖不是遗传物质,理由是什么?
_______________________________________________________________。
(5)肺炎双球菌具有的细胞器是________。
如图是动物体细胞有丝分裂的模式图,但是其中有两幅图是错误的。则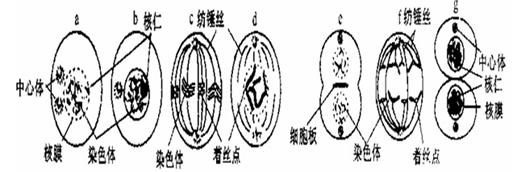
⑴a~g中错误的图片是和,前者错在,后者错在。
⑵从a~g中选出正确的图片后,将它们按照细胞分裂的先后顺序进行排列,其中排在第3位的图片是。
⑶b图所示细胞处于期,该期发生的分子水平的变化是。
⑷据图判断该动物体细胞的染色体数是条。
、某致病细菌分泌的外毒素无色、细针状结晶,对小鼠和人体有很强的毒性,可引起流涎、呕吐、便血、痉挛等,,该毒素为环状肽,结构式如下图所示: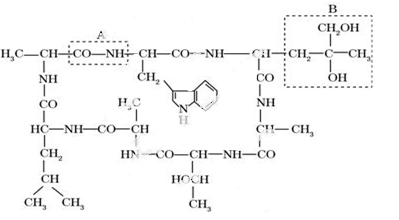
请据图分析回答:
⑴该化合物中含有游离的____个氨基,_____个羧基。
⑵该化合物是由____个氨基酸组成的,区别这些氨基酸的种类是依靠其结构中的______。
⑶组成该化合物的氨基酸有____种,其中有____个氨基酸的R基相同,这个R基是_____。
⑷该化合物称为_____肽化合物,含有_____个肽键。
⑸填写虚线框内结构的名称:A:______B:______(从氨基酸的结构通式的角度讲)
(6)该化合物具有8个氮原子,其中_____个位于肽键上,______个位于R基上。
(7)该外毒素环肽在形成过程中失去了______个水分子。