如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是
| A.质子透过离子交换膜由右向左移动 |
| B.铜电极应与X相连接 |
| C.M电极反应式:(C6H10O5)n+7nH2O-24ne-=6nCO2↑+24n H+ |
| D.当N电极消耗0.25 mol气体时,则铁电极增重16 g |
下列各组物质中,每种物质都是既有离子键又有共价键的一组是
| A.NaOH H2SO4 (NH4)2SO4 | B.MgO Na2SO4 HNO3 |
| C.Na2O2 KOH Na3PO4 | D.HCl Na2O MgCl2 |
下列离子方程式正确的
A.将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO +OH- = CaCO3↓+H2O +OH- = CaCO3↓+H2O |
| B.Fe(OH) 3溶于氢碘酸:2Fe(OH)3 + 6H+ + 2Iˉ = 2Fe2+ + I2 + 6H2O |
| C.向硫酸铝铵[NH4Al(SO4) 2]溶液中加入氢氧化钡溶液至SO42ˉ离子沉淀完全Al3+ + 2SO42ˉ + 2Ba2+ + 4OHˉ= AlO2ˉ + 2BaSO4↓+ 2H2O |
| D.4mol·L-1的NaAlO2溶液和7mol·L-1的HCl等体积互相均匀混合AlO2-+ H+ + H2O = Al(OH)3↓ |
下图是CO2电催化还原为CH4的工作原理示意图。下列说法正确的是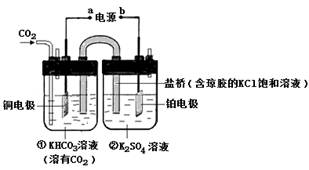
| A.该过程是化学能转化为电能的过程 |
| B.一段时间后,①池中n(KHCO3)不变 |
| C.一段时间后,②池中溶液的pH一定增大 |
| D.铜电极的电极反应式为CO2+6H2O+8e-=CH4+8 OH— |
下列实验能达到目的的是
X、Y、Z、W、U是分别位于短周期的元素,原子序数依次递增。X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13。Y元素的单质在X的某种氧化物中可燃。下列说法正确的是
| A.W的最高价氧化物能与水反应生成相应的酸 |
| B.Y、Z元素的单质作电极,在NaOH溶液环境下构成原电池,Z电极上产生大量气泡 |
| C.室温下,0.05 mol/L U的气态氢化物的水溶液的pH > 1 |
| D.Y、Z、U元素的简单离子半径由大到小的顺序: Y > Z > U |