下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②Na2O2投入FeCl2溶液中
③过量NaOH溶液和明矾溶液混合
④NaAlO2溶液和NaHCO3溶液混合
| A.只有①② | B.只有④ |
| C.只有③④ | D.只有①②④ |
β--紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。
下列说法正确的是( )
| A.β--紫罗兰酮可使酸性KMnO4溶液褪色 |
B.1mol中间 体X最多能与2mol H2发生加成反应 体X最多能与2mol H2发生加成反应 |
| C.维生素A1易溶于NaOH溶液 |
| D.β--紫罗兰酮与中间体X互为同分异构体 |
以乙醇为原料,用下述6种类型的反应:(1)氧化;(2)消去;(3)加成;(4)酯化;(5)水解;(6)加聚,来合成乙二酸乙二酯(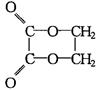 )的正确顺序是( )
)的正确顺序是( )
| A.(1)(5)(2)(3)(4) | B.(1)(2)(3)(4)(5) |
| C.(2)(3)(5)(1)(4) | D.(2)(3)(5)(1)(6) |
下列有机物中,在不同条件下,既能发生水解反应和消去反应,又能发生酯化反应并能与金属钠反应放出氢气的是( )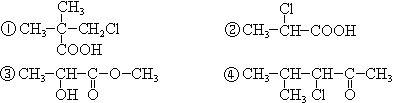
| A.只有② | B.只有①② | C.只有②③ | D.只有①②③ |
烯烃、一氧化碳和氢气在催化剂作用下生成醛的反应,称为羰基合成,也叫烯烃的醛化反应。由乙烯制丙醛的反应为:CH2=CH2+CO+H2  CH3CH2CHO。由化学式为C4H8的烯烃进行醛化反应,得到的醛的同分异构体可能有 ( )
CH3CH2CHO。由化学式为C4H8的烯烃进行醛化反应,得到的醛的同分异构体可能有 ( )
| A.2种 | B.3种 | C.4种 | D.5种 |
下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:2的是()