下列热化学方程式中,正确的是
| A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为 CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol,则H2SO4和Ca(OH)2反应的中和热 ΔH=2×(-57.3)kJ·mol-1 |
D.500℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g)放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 kJ·mol-1 |
下列说法中正确的是
| A.化学键只能使原子相结合, 不能使离子相结合. |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因. |
| C.烷烃CH3(CH2)3CH3沸点比(CH3)2CHCH2CH3的低 |
| D.天然气﹑石油和水煤气分别属于化石能源﹑可再生能源和二次能源. |
已知H+ +OH- = H2O生成1 mol H2O放出热量57.3 kJ,下列反应中放出57.3 kJ热量的是
A.1 mol稀 H2SO4与足量NaOH溶液反应 H2SO4与足量NaOH溶液反应 |
| B.稀盐酸与氨水反应生成1 mol H2O |
| C.稀盐酸与稀Ba(OH)2溶液反应生成1 mol水 |
| D.稀NaOH与98.3%硫酸生成1 mol水 |
下列分子式表示的物质,具有同分异构体的是
| A.C3H7Cl | B.C3H8 | C.CH2Cl2 | D.CH4O |
下列反应中,既属于氧化还原反应同时又是吸热反应的是
| A.Ba(OH)2.8H2O与NH4Cl反应 | B.铝与稀盐酸 |
| C.灼热的炭与CO2反应 | D.甲烷与O2的燃烧反应 |
下列说法中正确的一组是
| A.H2和D2互为同位素 |
B.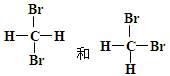 互为同分异构体 互为同分异构体 |
| C.正丁烷和异丁烷是同系物 |
D. 是同一种物质 是同一种物质 |