下图表示反应N2(g)+3H2(g) 2NH3(g)ΔH=-92.2kJ/mol。在某段时间t0~t6中反应速率与反应过程的曲线图如下,则氨的百分含量最高的一段时间是
2NH3(g)ΔH=-92.2kJ/mol。在某段时间t0~t6中反应速率与反应过程的曲线图如下,则氨的百分含量最高的一段时间是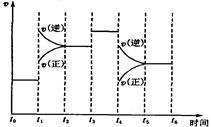
| A.t0~t1 | B.t2~t3 |
| C.t3~t4 | D.t5~t6 |
电化学腐蚀的本质是
| A.氧化还原反应 | B.酸碱中和反应 | C.置换反应 | D.分解反应 |
下列物质中,不属于合成材料的是
| A.塑料 | B.棉花 | C.合成纤维 | D.合成橡胶 |
光导纤维的主要成分是
| A.硅 | B.玻璃 | C.二氧化硅 | D.沙子 |
下列对合金描述不正确的是
| A.合金最多只能含有两种元素 |
| B.多数合金的硬度较大 |
| C.多数合金的熔点比成分金属低 |
| D.合金的性能跟合金元素的种类有关 |
下列叙述正确的是
| A.向体积为Va的0.02mol·L-1CH3COOH溶液中加入体积为Vb的0.02mol·L-1NaOH溶液,Va>Vb时:c(CH3COOH)+c(CH3COO-)>c (Na+) |
| B.将0.2 mol·L-1的盐酸与0.1 mol·L-1的KAlO2溶液等体积混合,其溶液中离子浓度由小到大的顺序为:c(OH-)<c(Al3+)<c(H+)<c(K+)<c(Cl-) |
| C.pH=5的HCOOH溶液和pH=5的NH4NO3溶液中,c(H+)不相等 |
| D.25℃时,pH=4,浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |