在某无色透明的酸性溶液中,能共存的离子组是
| A.Cu2+、K+、SO42-、NO3- | B.Na+、 K+、Cl-、 NO3- |
| C.Na+、K+、SO42-、HCO3- | D.Fe3+、K+、SO42-、Cl- |
有机物C4H8Cl2的同分异构体中只含一个“—CH3”的有
| A.2种 | B.3种 | C.4种 | D.5种 |
由CH3CH3→CH3CH2Cl→CH2 = CH2→CH3CH2OH的转化过程中,经过的反应是
| A.取代→消去→加成 | B.裂解→取代→消去 |
| C.取代→加成→氧化 | D.取代→消去→水解 |
有关溴乙烷的下列叙述中,正确的是
| A.溴乙烷不溶于水,其密度比水的小 |
| B.在溴乙烷中滴入AgNO3溶液,立即有淡黄色沉淀生成 |
| C.溴乙烷与NaOH的醇溶液混合共热可生成乙烯 |
| D.溴乙烷通常用乙烷与液溴直接反应来制取 |
下列化学用语正确的是
A.CH4分子的球棍模型: |
B.乙烯的结构简式:CH2CH2 |
| C.氯化钠的分子式:NaCl | D.K+的结构示意图: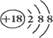 |
下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是
| A.CH3Cl |
B.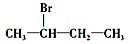 |
C.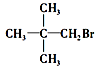 |
D.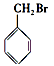 |