2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:
PCl3(g)+Cl2(g)= PCl5(g);反应达到平衡时,PCl5为0.4mol;如果此时移走1.0molPCl3和0.5molCl2,在相同的温度下再达到平衡时,PCl5的物质的量为
| A.0.4mol | B.0.2mol |
| C.小于0.2mol | D.大于0.2mol,小于0.4mol |
下表中第I栏中的化学反应和与第II栏中的化学反应都可以用第III栏中的离子方程式表示的是
| 选项 |
第I栏 |
第II栏 |
第III栏 |
| A |
NaHCO3溶液滴入Ca(OH)2溶液 |
NaHCO3溶液滴入NaOH溶液 |
OH-+HCO3-=CO32-+H2O |
| B |
铝片投入少量NaOH溶液 |
铝片溶液投入过量NaOH溶液 |
2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ |
| C |
碳酸钙加入足量稀盐酸 |
碳酸钠加入足量稀盐酸 |
CO32-+2H +=CO2↑+ H2O |
| D |
过量SO2气体通入NaOH溶液 |
少量SO2气体通入NaOH溶液 |
SO2+2OH-= SO32-+ H2O |
下列过程中,最终的白色沉淀不一定是BaSO4的是 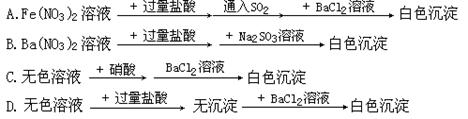
把等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,经充分搅拌后,将所得溶液用石墨做电极进行电解,阳极生成的物质是:
| A.H2 | B.Ag | C.Cl2 | D.O2 |
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是
A.K+、Na+、HCO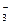 、NO 、NO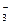 |
B.Na+、SO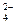 、Cl—、ClO— 、Cl—、ClO— |
C.H+、Mg2+、SO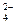 、NO 、NO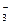 |
D.Ag+、K+、NO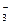 、Na+ 、Na+ |
将铜片和铝片用导线连接后插入盛有浓硝酸的烧杯中组成原电池,此原电池的负极及其电极反应分别是
| A.Al, Al- 3e-=Al3+ | B.Cu, Cu-2e-=Cu2+ |
| C.Al, 2H++2e-=H2↑ | D.Cu, 2H++NO3-+e-=NO2↑+H2O |