在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表: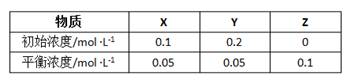
下列说法错误的是
| A.反应达到平衡时,X的转化率为50% |
B.反应可表示为X+3Y 2Z,其平衡常数为1600 2Z,其平衡常数为1600 |
| C.增大压强可使平衡向生成Z的方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
下列叙述正确的是
| A.浓度均为0.1 mol·L-1的下列溶液,pH由大到小的排列顺序为:NaOH>Na2CO3>(NH4)2SO4>NaHSO4 |
| B.为确定H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH >7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.常温下,将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液的pH=4 |
| D.常温下KSP(AgCl)=1.5×10-4,此时将足量氯化银固体分别投入相同体积的①蒸馏水②0.1mol/L盐酸③0.1 mol/L氯化镁溶液④0.1 mol/L硝酸银溶液中,则溶液中Ag+浓度:①>④=②>③ |
已知有机物A、B之间存在如右转化关系: (已配平)。则符合条件的B的结构最多有(不考虑立体异构)
(已配平)。则符合条件的B的结构最多有(不考虑立体异构)
A.5种B.6种C.7种D.8种
下列离子方程式书写正确的是
| A.澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| B.明矾溶液中滴加Ba(OH)2溶液至SO42–恰好完全沉淀:Al3++Ba2++ SO42–+3OH–=BaSO4↓+Al(OH)3↓ |
| C.200 mL 2 mol·L–1的FeBr2溶液中通入11.2 L标准状况下的氯气:4 Fe2++6Br–+5Cl2=4Fe3++3Br2+ 10Cl– |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO–+2Fe(OH)3=2FeO42–+3Cl–+H2O+4H+ |
下列说法正确的是
| A.1L 1mol•L-1的NH4Cl溶液中一定含有NA个NH4+ |
| B.常温常压下,22.4L乙烯中含极性共价键数为5 NA |
| C.6.8g熔融的KHSO4中含有0.05 NA个阳离子 |
| D.1mol冰醋酸和lmo1乙醇在浓硫酸加热下反应可生成NA个H2O |
下列说法正确的是
| A.地沟油和矿物油都属于酯类物质 |
| B.高温加热铝箔至熔化,铝并不滴落,说明铝表面有一层致密的耐高温氧化膜 |
| C.为测定熔融氢氧化钠的导电性,将氢氧化钠固体放在石英坩埚中加热熔化 |
| D.电解从海水中得到的氯化镁溶液可获得金属镁 |