下列说法正确的是( )
| A.1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热 |
| B.强酸和强碱的稀溶液发生中和反应一定是放热反应,弱酸和弱碱反应一定也是放热反应 |
| C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应 |
| D.酸和碱发生中和反应生成1 mol 水,这时的反应热叫中和热 |
依据下列说法来判断相应元素的金属性、非金属性强弱,不合理的是
| A.卤素单质Cl2、Br2、I2的氧化性强弱 |
| B.气态氢化物NH3、H2O、HF的稳定性 |
| C.碱金属单质Li、Na、K与水反应的剧烈程度 |
| D.1mol Na、Mg、Al分别与足量盐酸反应时失电子数的多少 |
油脂是重要的工业原料.关于“油脂”的叙述错误的是
| A.不能用植物油萃取溴水中的溴 |
| B.皂化是高分子生成小分子的过程 |
| C.和H2加成后能提高其熔点及稳定性 |
| D.水解可得到丙三醇 |
用惰性电极电解 2L1mol·L-1的硫酸铜溶液,在电路中通过 0.5mol电子后,将电源反接,电路中又通过 1mol电子,此时溶液中c(H+)是(设溶液体积不变) ()。
| A.1.5mol·L-1 | B.0.5mol·L-1 | C.0.75mol·L-1 | D.0.25mol·L-1 |
如下图所示,下列叙述正确的是()
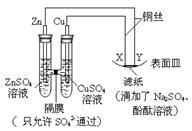
| A.Y为阴极,发生还原反应 | B.X为正极,发生氧化反应 |
| C.Y与滤纸接触处有氧气生成 | D.X与滤纸接触处变红 |
在1LK2SO4和CuSO4的混合溶液中,c(SO42-)=2.0mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标准状况)气体,则原溶液中K+的物质的量浓度为()
| A.2.0mol·L-1 | B.1.5mol·L-1 | C.1.0mol·L-1 | D.0.5mol·L-1 |