下列实验操作或对实验事实的叙述中存在错误的是 ( )
| A.用50mL酸式滴定管准确量取23.20mL酸性KMnO4溶液,放入锥形瓶中待用 |
| B.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| C.酸碱中和滴定时,锥形瓶未用待装液润洗。 |
| D.用惰性电极电解NaCl溶液,一段时间后,再加盐酸,可使溶液与原溶液完全一样。 |
下图中所示的实验方法、装置或操作完全正确的是

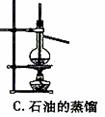

下列所发生的化学反应和实验室用乙醇和浓硫酸制乙烯的化学反应类型相同的是
| A.乙烯能使溴水褪色 |
| B.溴乙烷在NaOH的乙醇溶液中的反应 |
| C.用乙酸和乙醇在浓硫酸的作用下制乙酸乙酯 |
| D.乙醛能将新制的Cu(OH)2还原成Cu2O |
下表中实验操作能达到实验目的的是
| 实验操作 |
实验目的 |
|
| A |
向甲酸钠溶液中加新制的Cu(OH)2并加热 |
确定甲酸钠中含有醛基 |
| B |
向苯酚的饱和溶液中滴加少量稀溴水 |
制备三溴苯酚 |
| C |
向酒精和醋酸的混合液中加入金属钠 |
确定酒精中混有醋酸 |
| D |
将溴乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 |
检验水解产物中的溴离子 |
下列说法正确的是
| A.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
| B.蔗糖是高分子化合物,其水解产物能发生银镜反应 |
| C.淀粉和纤维素都可以作为工业上生产葡萄糖的原料 |
| D.蛋白质溶液中加入BaCl2溶液析出沉淀,此过程叫盐析 |
下列各组物质中,一定属于同系物的是
| A.HCHO、CH3COOH |
B. 、 、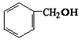 、 、 |
| C.C2H4、C6H12 |
| D.乙酸、硬脂酸 |