关于溶液中所含离子的检验,下列判断正确的是
| A.向溶液中加入BaCl2溶液,生成白色沉淀,加稀硝酸沉淀不溶解,则原溶液中一定含有SO42- |
| B.向溶液中滴加浓NaOH溶液并加热,产生的气体能使湿润的蓝色石蕊试液变红,则原溶液中一定含有NH4+ |
| C.向溶液中加入几滴KSCN溶液,溶液不显红色,再向溶液中加几滴新制氯水,溶液变为血红色,该溶液中一定含有Fe2+ |
| D.向溶液中滴加稀盐酸产生无色无味气体,产生的气体能使澄清石灰水变浑浊,则原溶液中一定有CO32- |
只用下列一种试剂,就能将Ba(NO3)2、NaAlO2、NaHCO3、AlCl3四种无色透明溶液区别开来,这种试剂是 ( )
| A.硫酸 | B.盐酸 | C.氨水 | D.氢氧化钠溶液 |
能正确表示下列反应的离子方程式的是( )
| A.硫酸铝溶液中加入过量氨水 Al3++3OH-=Al(OH)3↓ |
| B.碳酸钠溶液中加入澄清石灰水 Ca(OH)2+ CO32-=CaCO3↓+2OH- |
| C.冷的氢氧化钠溶液中通入氯气 Cl2+2OH-=ClO-+Cl-+H2O |
| D.稀硫酸中加入铁粉 2Fe+6H+=2Fe3++3H2↑ |
下列关于碳和硅的叙述中,正确的是( )
| A.其氧化物都能与NaOH溶液反应 |
| B.其单质在加热时都能跟O2反应 |
| C.其氧化物都能溶于水生成相应的酸 |
| D.碳和硅两种元素共有两种单质 |
在1 L 1 mol·L-1的氨水中,下列说法正确的是()
| A.含有1 mol NH3分子 | B.含NH3和NH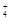 之和为1 mol 之和为1 mol |
| C.含NH3·H2O 1 mol | D.含NH3、NH3·H2O、NH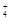 之和为1 mol 之和为1 mol |
下列金属冶炼的反应原理,错误的是 ( )
A.2NaCl(熔融) 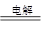 2 Na+Cl2↑ 2 Na+Cl2↑ |
B.MgO+H2 Mg+H2O Mg+H2O |
C.Fe2O3+3CO  2Fe+3CO2 2Fe+3CO2 |
D.2HgO 2Hg+O2↑ 2Hg+O2↑ |