在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐”(BrO3-)这一潜在致癌物质被做了严格限制。有关专家解释,矿泉水在开采过程中会含有少量溴化物(O3),在后续的生产过程中经臭氧(O3)处理逐渐转化为溴酸盐。下列有关该转化过程的认识正确的是
| A.该过程中溴化物(Br-)得到电子 |
| B.该过程中溴元素被还原,氧元素被氧化 |
| C.该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂 |
| D.该过程中溴元素发生氧化反应,氧元素发生还原反应 |
下列说法正确的是
| A.某晶体固态不导电,水溶液能导电说明该晶体是离子晶体 |
| B.原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力 |
| C.分子组成相差一个或几个CH2原子团的有机物是同系物 |
| D.在氢原子的基态电子的概率分布图中,小黑点的疏密程度表示电子在该区域空间出现概率的大小 |
能够快速、微量、精确的测定相对分子质量的物理方法是
| A.质谱 | B.红外光谱 | C.紫外光谱 | D.核磁共振谱 |
节日期间对大量盆栽鲜花施用S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如下图,下列说法正确的是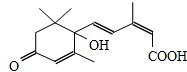
| A.1mol该分子可与1molNa发生反应产生H2 |
| B.分子中含有两种官能团 |
| C.可发生加成反应和取代反应 |
| D.该分子不能使酸性高锰酸钾溶液褪色 |
烷基取代苯 可以被KMnO4的酸性溶液氧化生成
可以被KMnO4的酸性溶液氧化生成 ,但若烷基R中直接与苯环连接的碳原子上无C-H键,则不被氧化,现有分子式是C12H18的二烷基取代苯则它可以被氧化为
,但若烷基R中直接与苯环连接的碳原子上无C-H键,则不被氧化,现有分子式是C12H18的二烷基取代苯则它可以被氧化为 的异构体有
的异构体有
| A.13种 | B.14种 | C.15种 | D.16种 |
下列各组烃的混合物,只要总质量一定,按任意比例混合,完全燃烧后生成的CO2和H2O都是恒量的是
| A.C2H2、C2H4 | B.C2H4、C4H6 |
| C.C2H6、C3H6 | D.C6H6、C2H2 |