某同学按如下图所示的装置进行实验。A、B为两种常见金属,它们的硫酸盐可溶于水。当 K 闭合时,在交换膜处 SO42一从右向左移动。下列分析正确的是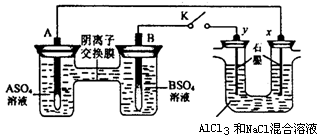
A.溶液中c(A2+)减小
B.B的电极反应:B-2e- =B2+
C.y电极上有H2产生,发生还原反应
D.反应初期,x电极周围出现白色胶状沉淀,一段时间以后沉淀逐渐溶解
下列有机知识正确的有_____个
① 名称:2,3—二甲基—1,5—戊二烯 ②乙烯的实验式;CH2
名称:2,3—二甲基—1,5—戊二烯 ②乙烯的实验式;CH2
③用质谱仪和红外光谱均可以获得有机物所含化学键或官能团信息
④乙醇的分子式:C2H5OH ⑤苯乙炔共线的原子最多有6个
⑥对甲基苯甲醇的结构简式:
| A.2个 | B.3个 | C.4个 | D.5个 |
把锌片和铁片放在盛有食盐水和酚酞试液的表面皿中,装置如下图。观察到溶液首先变红色的区域是
| A.Ⅰ和Ⅲ | B.Ⅰ和Ⅳ | C.Ⅱ和Ⅲ | D.Ⅱ和Ⅳ |
电解装置如图所示。图中B装置盛1000mL 3mol·L-1Na2SO4溶液,A装置中盛1000mL 3mol·L-1AgNO3溶液。通电一段时间后,润湿的淀粉KI试纸的C端变蓝色。室温下,若从电解开始到时间为t时,A、B装置中共收集到16. 8 mL(标准状况)气体。若电解过程中无其他副反应发生,且溶液体积变化忽略不计,下列判断正确的是
A. 电子流动的方向:Fe→Pt→石墨→Cu
B. B中石墨上可能有红色物质析出
C. 若把Fe电极改成Ag电极,可向Pt上镀银
D. t时A溶液的pH为3
下列用来表示物质变化的化学用语中,错误的是
| A.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| B.粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu2+ +2e- =Cu |
C.用Pt电极电解氯化铝溶液:2Cl-+2 H2O  Cl2↑+H2+2OH- Cl2↑+H2+2OH- |
| D.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O |
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:
电池:Pb(s) + PbO2(s) + 2H2SO4(aq) =2PbSO4(s) + 2H2O(l)
电解池:2Al+3H2O  Al2O3+3H2↑
Al2O3+3H2↑
电解过程中,以下判断正确的是
| 电池 |
电解池 |
|
| A |
H+移向Pb电极 |
H+移向Pb电极 |
| B |
每消耗3molPb |
生成2molAl2O3 |
| C |
正极:PbO2+4H++2e-=Pb2++2H2O |
阳极:2Al+3H2O-6e-=Al2O3+6H+ |
| D |
 |
 |