燃烧a g乙醇(液态),生成二氧化碳气体和27g液态水,放出的热量为Q kJ,则表示乙醇燃烧热的热化学方程式书写正确的是
| A.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1);△H = -QkJ/mol |
| B.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1);△H =" -Q/2" kJ/mol |
| C.1/2 C2H5OH(1)+3/2O2(g)=CO2(g)+3/2H2O(1);△H =" -Q" kJ/mol |
| D.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1);△H =" -2Q" kJ/mol |
下列陈述Ⅰ、Ⅱ均正确且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
Fe3+有氧化性 |
FeCl3溶液可溶解废旧电路板中的铜 |
| B |
SiO2有导电性 |
SiO2可用于制备光导纤维 |
| C |
NH3有还原性 |
NH3可用H2SO4吸收 |
| D |
浓HNO3有酸性 |
浓HNO3不可用铁制容器盛放 |
在pH =1且含有大量Fe2+和NH4+的溶液中,能大量存在的阴离子是
| A.SO42- | B.NO3- | C.OH- | D.HCO3- |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.1 mol OH- 中含有9NA个电子 |
| B.28 g的CO气体中含有NA个氧原子 |
| C.1 L 1 mol/L的AlCl3溶液中含有NA个Al3+ |
| D.常温常压下11.2 L的甲烷气体含有的分子数为0.5NA |
下列说法中,正确的是
| A.稀硫酸不具有氧化性 |
| B.NH4Cl中只含有离子键 |
| C.可用丁达尔效应区分溶液和胶体 |
| D.金属阳离子被还原时一定得到金属单质 |
下列化学用语正确的是
| A.钙离子的电子式:Ca2+ |
B.HCl的电子式: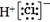 |
C.中子数为20的氯原子: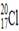 |
D.O的原子结构示意图: |