固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如图所示:

根据上述实验,以下说法正确的是( )
| A.溶液甲中一定含有K2SiO3、NaNO2 |
| B.无法判断溶液中是否有K2SO3 |
| C.气体A和气体B-定为混合物 |
| D.原混合物中一定有Fe2O3 |
现代化学测定有机化合物结构的分析方法比较多,经常采用的是1H核磁共振(1H–NMR)、红外光谱(IR)等方法。在1H–NMR分析中,有机物分子中的氢原子核所处的化学环境(即附近的基团)不同,表现出的核磁性不同,代表核磁性特征的峰在核磁共振谱图中横坐标的位置也就不同。下图1和图2是A、B两种物质的1H核磁共振氢谱。已知A、B两种物质都是烃类,都含有6个氢原子。请根据图1和图2两种物质的核磁共振氢谱图选择出不可能属于图1和图2的两种物质是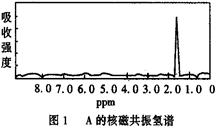

A.A是C3H6 ;B是C4H6B.A是C2H6 ;B是C3H6
C.A是C2H6 ;B是C6H6(苯)D.A是C3H6;B是C2H6
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中不正确的是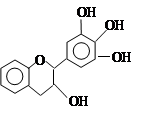
A.分子中所有的原子共平面
B.1mol EGC与含4mol NaOH的水溶液恰好完全反应
C.易发生氧化反应和取代反应,难发生加成反应
D.遇FeCl3溶液发生显色反应
某气态烃1 mol能与2 mol HCl完全加成,加成后产物分子上的氢原子又可被6 mol Cl2取代,则此气态烃可能是
| A.CH3—C≡C—CH3 | B.CH2=CH2 |
| C.CH≡C—CH3 | D.CH2=CH—CH3 |
下列实验方案合理的是
| A.除去苯中的少量苯酚:加入浓溴水振荡、静置后过滤,除去三溴苯酚沉淀 |
| B.检验酒精中的少量水:向酒精中加入足量生石灰 |
| C.制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 |
| D.除去乙烯中杂质气体:将实验室制得的乙烯气体通入NaOH 溶液 |
有一种有机物是由五个苯环相连形成的,因其分子结构酷似奥林匹克五环旗,科学家称其为奥林匹克烃(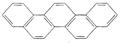 )。下列有关奥林匹克烃的说法正确的是
)。下列有关奥林匹克烃的说法正确的是
| A.该有机物属于芳香族化合物,是苯的同系物 |
| B.该烃既能发生氧化反应又能发生还原反应 |
C.该烃完全燃烧生成CO2与H2O的物质的量的关系满足: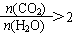 |
| D.该有机物的一氯代物只有一种 |