下列溶液中微粒的物质的量浓度关系正确的是 ( )
| A.在0.1mol/L NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-) |
| B.在0.1mol/L Na2CO3溶液中:2c(Na+)= c(HCO3-)+c(CO32-)+ c(H2CO3) |
| C.物质的量浓度相等的CH3COOK和CH3COOH溶液中,溶液显酸性:c(CH3COO-)>c(CH3COOH) |
| D.物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中的c(NH4+):①>②>③ |
下列归类中,正确的是
| A.Fe、Si——主族元素 | B.Na2O2——碱性氧化物 |
| C.阿司匹林——抗酸药 | D.醋——调味剂和防腐剂 |
下列说法正确的是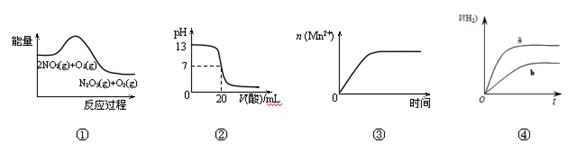
A.①表示化学反应2NO2(g) + O3(g)  N2O5(g) + O2(g)△H> 0 N2O5(g) + O2(g)△H> 0 |
| B.②表示25℃时,用0.1 mol/LCH3COOH溶液滴定20 mL 0.1 mol/LNaOH溶液,溶液的pH随加入酸体积的变化 |
| C.③表示10 mL 0.01 mol/L KMnO4酸性溶液与过量的0.1 mol/LH2C2O4溶液混合时,n (Mn2+)随时间的变化 |
| D.④表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。下列说法正确的是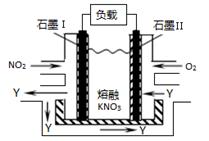
| A.O2在石墨Ⅱ附近发生氧化反应 |
| B.该电池放电时NO3-向石墨Ⅱ电极迁移 |
C.石墨Ⅰ附近发生的反应:3NO2 +2e- NO+ 2NO3- NO+ 2NO3- |
| D.相同条件下,放电过程中消耗的NO2和O2的体积比为4∶1 |
利用如图所示装置进行下列实验,不能得出相应实验结论的是
| 选项 |
① |
② |
③ |
实验结论 |
| A |
稀硫酸 |
Na2CO3 |
Na2SiO3溶液 |
非金属性:S>C>Si |
| B |
浓硫酸 |
蔗糖 |
溴水 |
浓硫酸具有脱水性、氧化性 |
| C |
浓硝酸 |
Fe |
NaOH溶液 |
说明铁和浓硝酸反应可生成NO2 |
| D |
浓氨水 |
生石灰 |
酚酞 |
氨气的水溶液呈碱性 |
X、Y、Z为短周期非金属元素,其相关性质如下,下列叙述正确的是
| 元素 |
X |
Y |
Z |
| 单质与H2反应条件 |
暗处爆炸 |
光照 |
高温、高压、催化剂 |
| 常温下氢化物水溶液的pH |
小于7 |
小于7 |
大于7 |
A.Z的氢化物分子间存在氢键B.最外层电子数Z>Y
C.气态氢化物的稳定性Y>X D.Y的含氧酸均为强酸