现有两种短周期主族元素X、Y,且在常温下X的单质呈气态,Y的单质呈固态。则下列推断不正确的是
| A.若X、Y位于第ⅠA族,则X、Y可能与氧元素形成原子个数比为1:1或2:1的化合物 |
| B.若X、Y位于第三周期,则X、Y形成的化合物可能是离子化合物,也可能是共价化合物 |
| C.若气态HnX的沸点高于HnY,则X、Y只能位于元素周期表的第ⅥA族 |
| D.若X,Y位于周期表的同一周期,则最高价含氧酸的酸性可能是HnXOm>HaYOb |
天然维生素P(结构如下)是一种营养增补剂。关于维生素P的叙述,错误的是()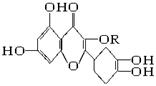
| A.可以和溴水反应 |
| B.可用有机溶剂萃取 |
| C.分子中有3个苯环 |
| D.1 mol维生素P可以和4 mol NaOH反应 |
对有机物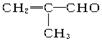 的化学性质的叙述,错误的是()
的化学性质的叙述,错误的是()
| A.既能发生氧化反应又能发生还原反应 |
| B.与H2发生加成反应,必定得一种纯的新有机物 |
| C.能发生加聚反应生成高聚物 |
| D.能使Br2的水溶液褪色,1 mol该有机物恰好与1 mol Br2反应 |
以下4种有机物的分子式都是C4H10O: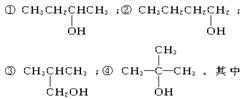
能被氧化为含相同碳原子数的醛的是()
| A.①② | B.只有② | C.②③ | D.③④ |
20世纪90年代,国际上提出了“预防污染”的根本手段发展“绿色化学”,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各环节都能实现净化和无污染的反应途径。下列各项属于“绿色化学”的是()
| A.处理废弃物 |
| B.治理污染点 |
| C.减少有毒源 |
| D.杜绝污染源 |
丁香油酚的结构简式是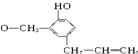 ,该物质不应有的化学性质是()
,该物质不应有的化学性质是()
①可以燃烧②可以跟溴加成③可以将酸性KMnO4溶液还原④可以跟NaHCO3溶液反应⑤可以跟NaOH溶液反应⑥可以发生消去反应
| A.①③ | B.③⑥ | C.④⑤ | D.④⑥ |