W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知
| A.Y元素氧化物对应水化物的酸性一定弱于Z |
| B.W、X、Y中最简单氢化物稳定性最强的是X |
| C.X元素形成的单核阴离子还原性大于Y |
| D.Z元素单质在化学反应中只表现氧化性 |
在标准状况下,mg气体A与ng气体B的分子数相同,下列说法不正确的是()。
| A.气体A与B的相对分子质量之比是m∶n |
| B.相同质量的气体A与B的分子数之比是n∶m |
| C.同温同压下气体A与B的密度之比为n∶m |
| D.相同状况下,同体积气体A与B的质量比为m∶n |
下列表示方法正确的是( )
A.NH4Br的电子式: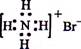 |
| B.S2-核外电子排布式:[Ne] 3s23p6 |
C.O原子处于基态的轨道表示式: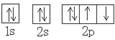 |
D.用电子式表示MgCl2的形成: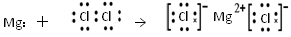 |
在多电子原子中,轨道能量是由以下哪些因素决定( )
①电子层②原子轨道类型③空间伸展方向④自旋状态
| A.①② | B.①④ | C.②③ | D.③④ |
现有CuO和Fe2O3组成的混合物a g,向其中加入2 mol·L—1的硫酸溶液50mL,恰好完全反应。若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量( )
| A.1.6 a g | B.(a-1.6) g | C.(a-3.2) g | D.a g |
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案一:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案二:铜铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是
| A.溶液A和溶液B均可以是盐酸或NaOH溶液 | B.若溶液B选用浓硝酸,测得铜的质量分数偏大 |
| C.方案一可能产生氢气,方案二可能剩余铜 | D.实验室中方案Ⅱ更便于实施 |