现代炼锌的方法可分为火法和湿法两大类,镉是生产硫酸锌的副产品,属于高毒性金属,试回答下列相关问题。
(1)火法炼锌是将闪锌矿(主要含ZnS)通过浮选、焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1373-1573K,使锌蒸馏出来。主要反应为:
2ZnS +3O2 2ZnO+2SO2;鼓风炉中:2C +O2
2ZnO+2SO2;鼓风炉中:2C +O2 2CO ZnO+CO
2CO ZnO+CO Zn + CO2
Zn + CO2
从火法炼锌蒸馏后的残渣中含多种金属单质及In2O3,可用硫酸提取铟,某研究机构对此研究数据如下。实验中涉及的酸度(每升溶液中含硫酸的质量)与铟的浸出率如下图1;硫酸溶液的体积与固体的体积比如图2

图1酸度对铟浸出率的影响 图2液固比对铟浸出率的影响
①当酸度为196时,其物质的量浓度为 。
②从节约原料和浸出率考虑,适宜的酸度和液固比分别为:_______、_______。
(2)湿法炼锌的主要工艺流程为:

①从保护环境和充分利用原料角度,如何处理或利用烟气 。
②除去酸浸出液中的铁,可用H2O2氧化,再调节pH使之形成Fe(OH)3沉淀,写出H2O2氧化Fe2+的离子方程式 。
③酸浸出液还含有Cd2+,为了防止镉污染并回收镉,根据它们性质的差异,可用氢氧化钠溶液分离,已知Zn(OH)2和氢氧化铝一样也具有两性,试写出分离的离子方程式__________、__________。
现有3种化合物 A、B、C均含短周期元素R,其转化关系如下图所示。
A、B、C均含短周期元素R,其转化关系如下图所示。
(1)若A由第三周期2种元素组成。常温下,0.1mol/L X溶液的pH=13,则R在周期中的位置是______________。X中阴离子的电子式是_________,B转化为C的离子方程式是___________。
(2)若常温下A、B、C、X均为气态物质,1mol A中含有共价键的数目约为1.806×1024,X为单质,A与X反应生成B的化学方程式是_____________;在一定条件下,A可与C反应消除C对大气的污染,该反应的化学方程式是________________。
书写下列化学反应方程式
(1)NO2与水反应
(2)C与浓硫酸反应
(3)Mg与CO2反应
书写下列离子反应方程式
(1)氯化铝与过量的氢氧化钠溶液反应
(2)NaAlO2溶液与足量的盐酸反应
(3)NaAlO2中通入过量的CO2气体
(4)FeCl3+H2S
(5)过量的Zn加入到FeCl3溶液中
(6)FeSO4+O2(酸性条件下)
(7)明矾净水
(14分) E是一种香料,可用下图的设计方案合成。
已知:A是一种饱和一氯代烃。
(1)A的结构简式为:。
(2)完成下列化学反应方程式为:
B→C:
B+D→E:
(3)F→G的化学反应类型是。
(4)写出检验C中官能团的化学反应方程式:。
(5)E有多种同分异构体,其中含有一个羧基,且其一氯代物有两种的是:
。(用结构简式表示)
(6分)有化合物: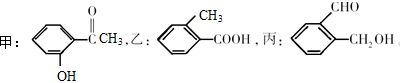
(1)请写出丙中含氧官能团的名称:______________。
(2)请判别上述哪些化合物互为同分异构体:_______ ___________________________。
___________________________。
(3)请按酸性由强到弱排列甲、乙、丙的顺序 。
。