最常见的塑化剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,反应的化学方程式及装置图(部分装置省略)如图:
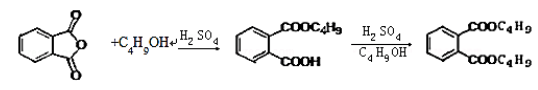

已知:正丁醇沸点118℃,纯邻苯二甲酸二丁酯是无色透明、具有芳香气味的油状液体,沸点340℃,酸性条件下,温度超过180℃时易发生分解。
由邻苯二甲酸酐、正丁醇制备邻苯二甲酸二丁酯实验操作流程如下:
① 向三颈烧瓶内加入30g(0.2mL)邻苯二甲酸酐,22g正丁醇以及少量浓硫酸。
② 搅拌,升温至105℃,持续搅拌反应2小时,保温至反应结束。
③ 冷却至室温,将反应混合物倒出,通过工艺流程中的操作X,得到粗产品。
④ 粗产品用无水硫酸镁处理至澄清→取清液(粗酯)→圆底烧瓶→减压蒸馏,经过处理得到产品20.85g。
请回答以下问题:
(1)步骤②中不断从分水器下部分分离出产物水的目的是 。判断反应已结束的方法是 。
(2)上述实验可能生成的副产物的结构简式为 (填一种即可)
(3)操作X中,应先用5%碳酸钠溶液洗涤粗产品,纯碱溶液浓度不宜过高,更不能使用氢氧化钠;若使用氢氧化钠溶液,对产物有什么影响?(用化学方程式表示) 。
(4)操作X中,分离出产物的操作中必须使用的主要玻璃仪器有 。
(5)粗产品提纯流程中采用减压蒸馏的目的是 。
(6)本实验中,邻苯二甲酸二丁酯(式量是278)的产率为 。
(18分,每小题2分)用质量分数为98%,密度为1.84g/cm3的浓硫酸来配置500ml,0.2mol/L的稀硫酸。可供选择①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙.请回答下列问题:
(1)上述仪器中,在配制稀硫酸时用不到的有(填代号).
(2)经计算,需浓硫酸的体积为mL(保留一位小数);。
(3)将浓硫酸加适量蒸馏水稀释后,冷却片刻,随后全部转移到mL的容量瓶中,转移时应用玻璃棒.转移完毕,用少量蒸馏水洗涤2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀.然后缓缓地把蒸馏水直接注入容量瓶直到液面接近瓶颈刻度cm处,改用滴加蒸馏水,使.塞上瓶塞、摇匀后,把溶液倒入试剂瓶、贴上标签.
(4)定容时,俯视刻度线,所配溶液的物质的量浓度将(选填“偏高”、“偏低”或“不变”)
(1)用50mL 0.50mol·L-1盐酸与50mL 0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题: 
①烧杯间填满碎泡沫塑料的作用是。
②若大烧杯上改为盖薄铁板,求得的反应热数值:(填“偏大”、“偏小”或“无影响”)
③若通过测定计算产生的热量为1.42kJ,请写该反应的热化学方程式:。
(2)①已知:CH4(g)+H2O(g)===CO(g)+3H2(g)ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g)ΔH=+247.4 kJ·mol-1
则以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:。
②由气态基态原子形成1 mol化学键释放的最低能量叫键能。已知表中所列键能数据, 则N2(g)+3H2(g) 2NH3(g) ΔH=kJ·mol-1。
2NH3(g) ΔH=kJ·mol-1。
| 化学键 |
H—H |
N—H |
N≡N |
| 键能kJ·mol-1 |
436 |
391 |
945 |
③一定条件下,在水溶液均为1 mol以下离子 Cl-、ClO-、ClO2-、ClO3-、ClO4-的能量(kJ)相对大小如下图所示,则3ClO-(aq)===ClO (aq)+2Cl-(aq)的ΔH=kJ·mol-1。
(aq)+2Cl-(aq)的ΔH=kJ·mol-1。
某化学兴趣小组想探究某一温度下氯化钠饱和溶液的酸碱度。探究过程如下:
【猜想或假设】溶液的pH可能为:①pH<7,②,③。
【设计和实验】要测定该溶液的酸碱度,除有正确的操作步骤外,其中不能采用下列物质中的(填序号)来进行实验。
①pH试纸②紫色石蕊试液③酚酞试液
组内同学进行了如下实验:
甲同学:取pH试纸放在玻璃片上,用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7。
乙同学:取pH试纸放在玻璃片上,先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7。
丙同学:将pH试纸直接浸入氯化钠溶液中,把试纸显示的颜色与标准比色卡比较,测得pH=7。
【评价与反思】三位同学中操作正确的是同学。
指出其于同学的操作错误:
同学:;
同学:;
【结论与分析】丙同学得出:“凡是盐溶液的pH都等于7”,你认为该同学结论
(填“正确”或“不正确”)。
如不正确,请举一例说明(如正确,该处不填)。
(本题包括2个小题,共18分)
19.某淡黄色的颗粒状固体,其化学性质比较活泼,在通常状况下能跟许多物质发生化学反应。例如:它与CO2反应时,只生成了Na2CO3和O2,它与稀盐酸反应时,只生成了NaCl、H2O和O2。上课时,老师做了如下实验:
a.取少量的淡黄色的颗粒状固体投入到盛有少量水的试管中,可观察到产生了一种无色无味的气体;
b.再向试管中滴加几滴酚酞试液,可观察到烧杯中溶液变红。
根据实验现象,回答下列问题:
(1)淡黄色的颗粒状固体中一定含有元素。你做出这个判断的理由是。
(2)实验a中产生的气体,可用法收集。
(3)同学们对实验a中产生的气体的组成看法不一,提出了以下几种假设:
①该气体是CO;②该气体是H2。
请你推测该气体还可能是(写化学式)。
(4)设计一个实验,证明你在(3)中的推测(写出简要操作步骤,反应现象和结论)。
| 操作步骤 |
|
| 反应现象 |
|
| 结论 |
现有失去标签的两瓶无色溶液:氯化钠溶液和稀盐酸。某化学探究小组打算用物理和化学两种方法加以区别。请回答:
(1)化学方法在不选用酸碱指示剂、pH试纸的情况下,按表中方法一(示例)填写。所选试剂须属于不同物质类别(单质、氧化物、酸、碱、盐、有机物等)。
| 所选试剂 |
判别方法 |
|
| 方法一 |
锌 |
取少量样品分别与锌反应,有气体产生的是稀盐酸,没有的是氯化钠溶液。 |
| 方法二 |
||
| 方法三 |
(2)物理方法同学小王使用了酒精灯和玻璃棒两种仪器,就把这两种无色溶液区分开了。请你猜测一下他的做法:
操作方法:
判断方法: