在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是
| A.X是电源的负极 |
| B.阴极的反应式是:H2O+2eˉ=H2+O2ˉCO2+2eˉ=CO+O2ˉ |
C.总反应可表示为:H2O+CO2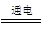 H2+CO+O2 H2+CO+O2 |
| D.阴、阳两极生成的气体的物质的量之比是1︰1 |
与100mL 0.5mol·L-1NaCl溶液中的Cl-的物质的量浓度相同的是
| A.100mL 0.5 mol·L-1MgCl2溶液 |
| B.100mL 0.5mol·L-1HCl溶液 |
| C.200mL 0.25 mo l·L-1 KCl溶液 |
| D.100mL 0.5mol·L-1NaClO溶液 |
下列关于胶体的叙述不正确的是
| A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间 |
| B.光线透过胶体时,胶体中可发生丁达尔效应 |
| C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 |
| D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| B.25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
| C.在常温常压下,11.2L Cl2含有的分子数为0.5NA |
| D.在标准状况下,11.2L H2O含有的分子数为0.5NA |
某盐的混合物中含有0.2mol Na+,0.4mol Mg2+,0.4mol Cl-,则SO42-为
| A.0.1mol | B.0.5mol | C.0.3mol | D.0.15mol |
下列物质按一定的分类方法属于同一类的是
| A.标准状况下的状态:O2、N2、NO、H2O | B.酸性氧化物:CO2、SO2、Cl2O7、N2O5 |
| C.非电解质:酒精、蔗糖、葡萄糖、醋酸 | D.混合物:液氯、盐酸、漂白粉、氯水 |