进行物质导电性实验测定时,按照图a、图b分别接通线路,下列叙述正确的是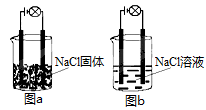
| A.NaCl是电解质,图a、图b灯泡均会发光 |
| B.图a灯泡不会发光,NaCl固体中不含Na+、Cl— |
| C.NaCl溶液在通电后发生:NaCl═Na+ +Cl— |
| D.通电前图b溶液由大量H2O、Na +、Cl—构成 |
下列关于乙酸性质的说法中,不正确的是
| A.易溶于水 | B.酸性比碳酸的酸性弱 |
| C.能发生酯化反应 | D.能和金属钠反应生成H2 |
下列化学用语正确的是
A.硫离子的结构示意图: |
B.氟化镁的电子式: |
| C.甘氨酸的结构式:C2H5O2N |
| D.氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH)22- |
下列分散系中,分散质粒子的直径在10-9~l0-7 m之间的是
| A.Fe(OH)3胶体 | B.氯化钠溶液 | C.硫酸铜溶液 | D.泥浆水 |
下列各组物质中,互为同分异构体的是
| A.冰和水 | B.氧气和臭氧 |
| C.1H与3H | D.CH3CH20H和CH30CH3 |
下列物质中,既能作为食品的防腐剂,又能作为食品的发色剂的是
| A.苯甲酸钠 | B.碳酸氢铵 | C.亚硝酸盐 | D.谷氨酸钠 |