某同学设计如下实验方案,以分离KCl 和BaCl2两种固体混合物,试回答下列问题:

(1)操作①的名称是 ,操作②的名称是 。
(2)试剂a是 ,试剂b是 ,固体B是 。(填化学式)
(3)加入试剂a所发生反应的化学方程式为: 。
加入试剂b所发生反应的化学方程式为: 。
(4)该方案能否达到实验目的: 。若不能,应如何改进(若能,此问不用回答) 。
(5)若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是 的质量。
利用过滤的方法可以初步除去粗盐中的泥沙等不溶性的杂质,但仍含有CaCl2,CaCl2是一种易溶于水的物质,无法用过滤的方式将其和NaCl分离,经过分析讨论,某小组同学在此基础上继续设计了如下实验:
回答下列问题:
(1)该小组同学的实验目的是;
(2)上图括号内的操作步骤 为①②;
为①②;
(3)按此实验方案得到的NaCl固体中肯定含有(填化学式)杂质,为了解决这个问题可以向过滤得到的滤液中加入适量的(填名称)。
(4)写出上述实验中加入过量Na2CO3后发生反应的化学方程式。
氮化铝是一种新型的无机非金属材料,被广泛应用于集成电路生产领域。在氮气流中由氧化铝与焦炭在电炉中加热制得。原料配比不当或反应不完全等因素都会造成产品中含有碳、Al4C3或Al2O3等杂质。回答下列问题:
(1)反应Al2O3+N2+ 3C  2AlN+3CO中,氧化剂是。
2AlN+3CO中,氧化剂是。
(2)AlN也可以与强碱溶液反应。完成下列方程式:
AlN+NaOH+H2O=+
(3)Al 4C3与水反应生成甲烷,反应方程式是
甲烷与CuO反应的化学方程式如下:
CH4+4CuO  CO2+2H2O+4Cu
CO2+2H2O+4Cu
为测定产品中有关成分的含量,所需仪器如下: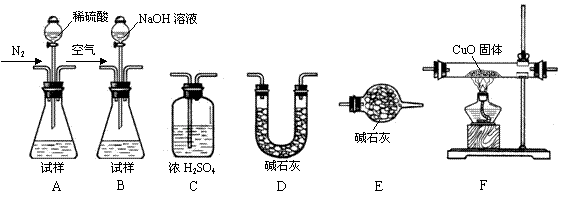 Ⅰ.测定样品中含有少量Al4C3的含量,各装置连接
Ⅰ.测定样品中含有少量Al4C3的含量,各装置连接 的顺序为A→C→F→C→D→E。主要实验步骤
的顺序为A→C→F→C→D→E。主要实验步骤 如下:
如下:
①称量D的质量,按顺序组装仪器,将试样放入锥形瓶中,检查装置的气密性
②从分液漏斗缓缓滴入稀硫酸,直到不再产生气体时为止
③点燃F酒精灯
④缓缓鼓入一定量的N2
⑤再次缓缓鼓入一定量的N2
⑥再次称量D的质量
⑦重复步骤⑤和⑥的操作,直到D的质量基本不变
操作的先后顺序是①→→⑤→⑥→⑦,操作④的目的是 。
。
Ⅱ.为测定AlN的含量,请选择合适的药品和装置,按气流方向连接各装置,其顺序为:
→→→E
若试样为mg,测得C增重n g,则AlN的质量分数是。
某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数。请回答:
(1)以上步骤有错误的是(填编号)_____,该错误操作会导致测定结果
(填“偏大”、“偏小”或“无影响”)__________________
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无影响”)___________________
(3)判断滴定终点的现象是:锥形瓶中溶液从色变为 色,且半分钟不变色。
(4)下图是某次滴定时的滴定管中的液面,其读数为mL
(5)根据下列数据:请计算待测盐酸溶液的浓度: mol/L
| 滴定次数 |
待测液体积(mL) |
标准烧碱体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.40 |
20.40 |
| 第二次 |
20.00 |
4.00 |
24.00 |
| 第三次 |
20.00 |
2.00 |
24.10 |
实验室用 98%、密度为1.84g/cm3的浓硫酸配制0.2mol/L的 H2SO4溶液1000mL.
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、、。
(2)其操作步骤可分解为以下几步:
A.用量筒量取mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,
并用玻璃棒搅拌。
B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里。
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里。
D.检查容量瓶是否漏水。
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处。
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液。
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切。
请据此填写:
①完成上述步骤中的空白处。
②补充完成正确的操作顺序(用字母填写):
( D  )→( A )→( C )→()→(
)→( A )→( C )→()→( )→()→( F )。
)→()→( F )。
③将浓硫酸在烧杯中稀释后移入容量瓶时,必须_________________ 方可移液.
方可移液.
(3)试分析下列操作对所配溶液的浓度有何影响
①量取浓硫酸时眼睛俯视刻度线,会导致所配溶液浓度会;(填:偏高、偏低、或无影响,下同)
②定容时,眼睛俯视刻度线,所配溶液浓度会;
③定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度。所配溶液浓度会.
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
(1)从氯化钠溶液中得到氯化钠固体,选择装置(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置;从碘水中分离出I2,选择装置,该分离方法的名称为。
(2)装置A中①的名称是,进冷却水的方向是。
装置B在分液时为使液体顺利下滴,应进行的具体操作是
 。(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用的方法除去
。(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用的方法除去
Fe(OH)3胶体中混有的杂质Cl-离子。