在恒容密闭容器中加入一定量的X并发生反应:2X(g) Y(g),在温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示。下列叙述正确的是
Y(g),在温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示。下列叙述正确的是

| A.该反应进行到N点放出的热量大于进行到W点放出的热量 |
B.T2下,在0 ~t1时间内,c(Y)=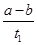 mol·L-1·min-1 mol·L-1·min-1 |
| C.W点的正反应速率V正大于N点的逆反应速率V逆 |
| D.W点时再加入一定量X,再达平衡后X的转化率减小 |
下列说法或表示方法正确的是()
| A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| B.由C(石墨)=C(金刚石);△H=+1.90 kJ/mol可知,金刚石比石墨稳定 |
| C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l);△H=-285.8kJ/mol |
| D.在稀溶液中,H+(aq)+ OH-(aq) = H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ |
下列方程式中,属于水解反应的是()
A.SO32-+H2O HSO3-+OH- HSO3-+OH- |
B.HCO3-+OH- H2O+CO32- H2O+CO32- |
C.CO2+H2O H2CO3 H2CO3 |
D.H2O+H2O H3O++OH- H3O++OH- |
已知反应X+Y= M+N为放热反应,对该反应的下列说法中正确的()
| A.X的能量一定高于M |
| B.X和Y的总能量一定高于M和N的总能量 |
| C.Y的能量一定高于N |
| D.因该反应为放热反应,故不必加热就可发生 |
下列事实中,不能用勒夏特列原理解释的是()
| A.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 |
| B.实验室中常用排饱和食盐水的方式收集氯气 |
| C.打开汽水瓶,有气泡从溶液中冒出 |
| D.对熟石灰的悬浊液加热,悬浊液中固体质量增加 |
下列说法正确的是()
| A.某物质的溶解性为难溶,则该物质不溶于水 |
| B.不溶于水的物质的溶解度为0 |
| C.绝对不溶解的物质是不存在的 |
| D.某离子被沉淀完全是指该离子在溶液中的浓度为0 |