污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略).
请回答下列问题:
(3)已知:25℃、101kPa时,
Mn(s)+O2(g)═MnO2(s)△H=-520kJ•mol-1
S(s)+O2(g)═SO2(g)△H=-297kJ•mol-1
Mn(s)+S(s)+2O2(g)═MnSO4(s)△H=-1065kJ•mol-1
SO2与MnO2反应生成无水MnSO4的热化学方程式是____________________________________。
(2)用离子方程式表示用MnCO3除去Al3+和Fe3+的原理(任选其一即可):_______________。
(3)用离子方程式表示用MnS除去Cu2+和Ni2+的原理(任选其一即可):___________________________。
(4)MnO2是碱性锌锰电池的正极材料.碱性锌锰电池放电时,正极的电极反应式是__________。
(5)MnO2可作超级电容器材料.用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是__________。
(6)假设脱硫的SO2只与软锰矿浆中MnO2反应.按照图示流程,将am3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为ckg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2____________kg。
某种利胆解痉药的有效成分是亮菌甲素,其结构简式如图所示。下列关于亮菌甲素的说法中,正确的是( )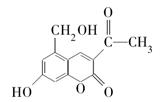
| A.亮菌甲素在一定条件下可以与乙酸发生酯化反应 |
| B.亮菌甲素的分子式为C12H12O5 |
| C.1 mol 亮菌甲素最多能和2 mol NaOH反应 |
| D.1 mol 亮菌甲素最多能和4 mol H2发生加成反应 |
化合物A(C11H8O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B和C。回答下列问题:
(1)B的分子式为C2H4O2,分子中只有一个官能团。则B的结构简式是________,B与乙醇在浓硫酸催化下加热反应生成D,该反应的化学方程式是________________,该反应的类型是________;写出两种能发生银镜反应的B的同分异构体的结构简式________________;
(2)C是芳香化合物,相对分子质量为180,其碳的质量分数为60.0%,氢的质量分数为4.4%,其余为氧,则C的分子式是________;
(3)已知C的芳环上有三个取代基,其中一个取代基无支链,且含有能使溴的四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是________。另外两个取代基相同,分别位于该取代基的邻位和对位,则C的结构简式是________________;
(4)A的结构简式是___________________。
相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示。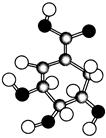
请回答下列问题:
(1)M的结构简式是________________________。
(2)下列关于M的说法,正确的是________。
A.遇FeCl3溶液呈紫色
B.遇紫色石蕊溶液变红色
C.遇溴水发生取代反应
D.能缩聚为高分子化合物
(3)M在一定条件下发生消去反应,生成 ,该反应的化学方程式是_________。
,该反应的化学方程式是_________。
(4)M与有机物A在一定条件下可生成一种相对分子质量为202的酯类物质。A可能的结构简式是______________________。
(5)研究发现,有一种物质B的分子组成和M完全一样,但分子中无环状结构;B在一定条件下水解能够产生甲醇;B的核磁共振氢谱如图(两个峰面积比为2∶3)。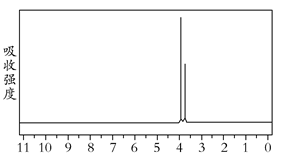
物质B的结构简式是____________。
对羟基苯甲酸丁酯(俗称尼泊金丁酯)可用作防腐剂。对酵母和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得。以下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
已知以下信息:
①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基;
②D可与银氨溶液反应生成银镜;
③F的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为1:1。
回答下列问题:
(1)A的化学名称为________;
(2)由B生成C的化学反应方程式为________,该反应的类型为________;
(3)D的结构简式为________;
(4)F的分子式为________;
(5)G的结构简式为________。
氯乙烷跟化合物之间的转化如图所示: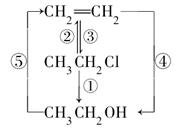
(1)写出各反应的化学方程式____________________________________。
(2)上述化学反应的反应类型有________,________,________。