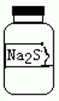
实验室一瓶固体M的标签右半部分已被腐蚀,剩余部分只看到“Na2S”字样(如图所示),已知,固体M只可能是Na2SO3、Na2SiO3、Na2SO4中的一种。 若取少量固体M配成稀溶液进行有关实验,下列说法不正确的是( )
| A.只用盐酸一种试剂就可以确定该固体M的具体成分 |
| B.往溶液中通入二氧化碳,若有白色沉淀,则固体M为Na2SiO3 |
| C.常温时用pH试纸检验,若pH=7,则固体M一定是Na2SO4 |
| D.往溶液中加入稀硝酸酸化的BaCl2,若有白色沉淀,则固体M为Na2SO4 |
为防止FeSO4被氧化而变质,实验室在配制FeSO4溶液时,常在溶液中加入少量的
| A.铜粉 | B.铁粉 | C.锌粉 | D.Fe2(SO4) |
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是
| A.加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B.加热时,②、③溶液均变红,冷却后又都变为无色 |
| C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅 |
| D.四个“封管实验”中所发生的化学反应都是可逆反应 |
下列分离提纯方法不正确的是
| A.分离KNO3和氯化钠,常用结晶与重结晶 |
| B.分离I2和NaI的混合物,常用升华法 |
| C.分离乙醇中和水的混合物,常用蒸馏法 |
| D.苯和酸性高锰酸钾溶液可用分液法 |
草酸溶液能使酸性KMnO4溶液褪色,其离子方程式为
MnO4-+H2C2O4+H+→CO2↑+Mn2++__(未配平)。关于此反应的叙述正确的是
| A.该反应的还原产物是CO2 |
| B.该反应右框内的产物是OH- |
| C.配平该反应后,H+计量数是6 |
| D.1molMnO4-在反应中失去5mol电子 |
某无色溶液可能含I-、NH4+、Cu2+、SO32-中的若干种,向溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32- ④可能含有I— ⑤可能含有SO32-
| A.②③④ | B.②④⑤ | C.①②⑤ | D.①②③ |