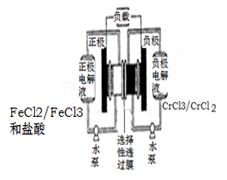
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为
Fe3++Cr2+ Fe2++Cr3+.下列说法一定正确的是( )
Fe2++Cr3+.下列说法一定正确的是( )
| A.氧化性:Cr3+>Fe3+ |
| B.电池放电时,负极的电极反应式为Fe2+﹣e﹣═Fe3+ |
| C.充电时,阴极的电极反应式为Cr3++e﹣═Cr2+ |
| D.电池放电时,Cl﹣从负极室穿过选择性透过膜移向正极室 |
某固体化合物A不导电,但熔化或溶于水都能完全电离。下列关于物质A的说法中,正确的是()
| A.A为非电解质 | B.A是强电解质 |
| C.A是离子晶体 | D.A是弱电解质 |
下列在指定溶液中的各组离子,能够大量共存是()
A.无色溶液中: 、Na+、Cl-、OH- 、Na+、Cl-、OH- |
B.pH=11的溶液中:S2-、K+、 、Cl- 、Cl- |
C.pH=1的溶液中:Fe2+、 、Mg2+、 、Mg2+、 |
D.水电离的c(H+)=10-12 mol·L-1的溶液中:Fe3+、 、K+、SCN- 、K+、SCN- |
将锌片跟醋酸溶液反应,若在溶液中加入固体醋酸钠,则生成氢气的速率会()
| A.增大 | B.减小 | C.不变 | D.先增大,后减小 |
对某弱酸稀溶液加热时,下列叙述错误的是()
| A.弱酸的电离程度增大 | B.弱酸分子的浓度减小 |
| C.溶液的c(OH-)增大 | D.溶液的导电性增强 |
把0.05 mol NaOH固体分别加入下列液体100 mL中,溶液的导电能力变化最小的是()
| A.自来水 | B.0.5 mol·L-1盐酸 |
| C.0.5 mol·L-1硝酸 | D.0.5 mol·L-1 NH4Cl |