温度和浓度均相同的下列溶液:①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4Cl、⑤NaClO⑥CH3COONa,它们的pH值由小到大的排列顺序是( )
| A.③①②④⑤⑥ | B.⑤⑥②④①③ | C.③①④②⑥⑤ | D.③①⑥④②⑤ |
已知H2(g)+Br2(l)═2HBr(g);△H=﹣72kJ/mol.蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
| H2(g) |
Br2(g) |
HBr(g) |
|
| 1mol分子中的化学键断裂时 需要吸收的能量/KJ |
436 |
a |
369 |
则表中a为( )
A.404B.260 C.230 D.200
已知:(1)H2(g)+ O2(g)═H2O(g);△H="a" kJ/mol
O2(g)═H2O(g);△H="a" kJ/mol
(2)2H2(g)+O2(g)═2H2O(g);△H="b" kJ/mol
(3)H2(g)+ O2(g)═H2O(l);△H="c" kJ/mol
O2(g)═H2O(l);△H="c" kJ/mol
(4)2H2(g)+O2(g)═2H2O(l);△H="d" kJ/mol
下列关系式中正确的是( )
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D.X和Y的总能量一定低于M和N的总能量 |
肯定属于同族元素且性质相似的是( )
| A.原子核外电子排布式:A为1s22s2,B为1s2 |
B.结构示意图:A为 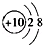 ,B为 ,B为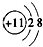 |
| C.A原子基态时2p轨道上有1个未成对电子,B原子基态时3p轨道上也有1个未成对电子 |
| D.A原子基态时2p轨道上有一对成对电子,B原子基态时3p轨道上也有一对成对电子 |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A.第一电离能Y可能小于X |
| B.气态氢化物的稳定性:HmY大于HnX |
| C.最高价含氧酸的酸性:X对应的酸性强于Y对应的 |
| D.X和Y形成化合物时,X显负价,Y显正价 |