室温下,pH相关2的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )
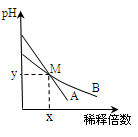
A.取等体积M点的A、B两种碱液加入同浓度的硫酸溶液至恰好完全反应时,所消耗酸溶液的体积相同
B.用醋酸中和A溶液至恰好完全反应时,溶液的pH不一定大于7
C.稀释前两溶液中H+浓度的大小关系:A=10B
D.稀释前,A溶液中由水电离出的OH-的浓度大于10-7mol/L
在实验室进行下列实验,括号内的实验仪器或试剂都能用到的是
| A.中和热的测定(量筒、温度计、酒精灯) |
| B.从溴水中提取溴单质(分液漏斗、无水乙醇、玻璃棒) |
| C.探究浓硫酸与铜反应的产物(蘸有碳酸钠溶液的棉花团、蒸馏水、烧杯) |
| D.制氢氧化铁胶体(饱和FeCl3溶液、NaOH溶液、胶头滴管) |
下列化学用语的使用正确的是
| A.硫酸酸化的淀粉KI溶液在空气中变成蓝色:4I-+O2+2H2O==2I2+4OH- |
| B.钢铁发生吸氧腐蚀时,正极的电极反应式:O2+4e-+2H2O==4OH- |
C.氨气催化氧化生产硝酸的主要反应:4NH3+7O2 4NO2+6H2O 4NO2+6H2O |
| D.向Na2SiO3溶液中通入过量CO2:SiO32-+2CO2+2H2O===H2SiO3+CO32- |
下表为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素。下列说法正确的是
| X |
||
| Y |
Z |
R |
| W |
A.五种元素的原子最外层电子数一定都大于2
B.X、Z原子序数可能相差18
C.Z可能是氯元素
D.Z的氧化物与X单质不可能发生置换反应
NA为阿伏加德罗常数的数值,下列说法正确的是
| A.7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA |
| B.0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1 NA |
C.反应3H2(g)+N2(g) 2NH3(g) ΔH=-92 kJ/mol放出热量9.2 kJ时,转移电子0.6 NA 2NH3(g) ΔH=-92 kJ/mol放出热量9.2 kJ时,转移电子0.6 NA |
| D.0.1 mol H2O2分子中含极性共价键数目为0.3 NA |
下列大小顺序比较错误的是
| A.热稳定性:Na2CO3> NaHCO3>H2CO3 |
| B.相同pH的溶液,加水稀释后的pH:H2SO4>HCl> CH3COOH |
| C.离子半径:K+> Na+>Mg2+ |
| D.结合H+能力:OH->ClO->NO3- |