下列由相关实验现象所推出的结论正确的是
| A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是
| 物质 |
杂质 |
除杂质应选用的试剂和操作方法 |
|
| A |
CO2 |
CO |
通入O2,点燃 |
| B |
NaOH固体 |
Na2CO3固体 |
加入过量盐酸,蒸发 |
| C |
Cu(NO3)2溶液 |
AgNO3溶液 |
加入过量的铜粉,过滤 |
| D |
KNO3溶液 |
KOH溶液 |
加入适量的CuSO4溶液,过滤 |
把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,则得反应后各物质的质量如下。下列说法中正确的是
| 物质 |
a |
b |
c |
d |
| 反应前的质量(g) |
6.4 |
3.2 |
4.0 |
2.8 |
| 反应后的质量(g) |
5.2 |
X |
7.2 |
2.8 |
A.a和c是反应物B.d一定是催化剂
C.X=2.0g D.该反应是化合反应
下列所示的图像能反映相对应实验的是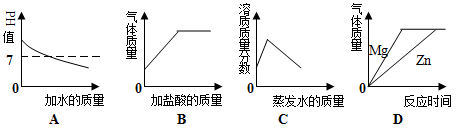
| A.向pH=13的NaOH溶液中不断加水稀释 |
| B.向碳酸氢钠溶液中逐滴加入稀盐酸至过量 |
| C.将60℃接近饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出 |
| D.将足量的金属镁片和锌片分别和等质量、相同质量分数的稀硫酸混合 |
有四种物质的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④CuCl2,不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是
| A.④①②③ | B.①③④② | C.④③②① | D.①④②③ |
将一定量的铁粉加入到一定量的硝酸银和硝酸镁的混合液中,充分反应后过滤,向滤渣中加入稀硫酸,有气泡产生,则在滤渣中
| A.一定有银、铁和镁 | B.仅有银和铁 |
| C.可能含镁 | D.只有银 |