下列关于电解质溶液的叙述正确的是( )
| A.室温下,pH=3的氢氟酸加水稀释后,电离常数Ka(HF)和pH均减小 |
| B.室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊试液呈红色 |
C.向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中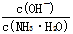 增大 增大 |
| D.室温下,将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)=c(NH4+) |
某元素原子核外电子排布为:第二层上的电子数比第一层与第三层电子数之和的两倍还多2,该元素是
| A.Na | B.Mg | C.Al | D.Cl |
现代科技将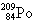 涂于飞机表面,可以吸收和屏蔽雷达波和红外线辐射,从而达到隐形目的。下面列出该原子核内中子数与核外电子数之差的数据正确的是
涂于飞机表面,可以吸收和屏蔽雷达波和红外线辐射,从而达到隐形目的。下面列出该原子核内中子数与核外电子数之差的数据正确的是
A.84B.41C.125 D.209
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3 + N2 + 3C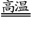 2AlN + 3CO↑
2AlN + 3CO↑
下列叙述不正确的是
| A.在氮化铝的合成反应中,N2是还原剂 |
| B.在氮化铝的合成反应中,C是还原剂 |
| C.氮化铝中氮元素的化合价为-3 |
| D.上述反应中每生成1molAlN,转移3 mol e- |
已知W、X、Y、Z四种短周期主族元素在周期表中的相对位置如右图所示,下列有关说法正确的是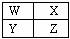
| A.Y的化学活泼性一定比W强 |
| B.Y元素的原子半径可能比X元素的原子半径小 |
| C.Z的气态氢化物的稳定性一定比X的强 |
| D.Z的原子序数可能是X的原子序数的2倍 |
已知短周期元素的离子aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则下列叙述正确的是
| A.原子半径:A﹥B﹥D﹥C | B.原子序数:d﹥c﹥b﹥a |
| C.离子半径:C﹥D﹥B﹥A | D.原子的最外层电子数目:A﹥B﹥D﹥C |