为了得到比较纯净的物质,使用的方法恰当的是( )
| A.向Na2CO3饱和溶液中,通入过量的CO2后,加热、蒸发得到NaOH晶体 |
| B.向Fe2(SO4)3溶液加入足量NaOH溶液,经过过滤、洗涤沉淀,再充分灼烧沉淀得Fe2O3 |
| C.向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体 |
| D.加热蒸发AlCl3饱和溶液得纯净的AlCl3晶体 |
化合物A(C4H8Br2)可由下列反应制得,C4H10O C4H8
C4H8 C4H8Br2,则A的结构式不可能的是()
C4H8Br2,则A的结构式不可能的是()
| A.CH3CH2CHBrCH2Br | B.CH3CH(CH2Br)2 | C.CH3CHBrCHBrCH3 | D.(CH3)2CBrCH2Br |
已知卤代烃可以和钠发生反应,例如溴乙烷与钠发生反应为:2CH3CH2Br + 2Na  CH3CH2CH2CH3 + 2NaBr应用这一反应,下列所给化合物中可以与钠合成环丁烷的是( )
CH3CH2CH2CH3 + 2NaBr应用这一反应,下列所给化合物中可以与钠合成环丁烷的是( )
| A.CH3Br | B.CH2BrCH2CH2Br | C.CH2BrCH2Br | D.CH3CH2CH2CH2Br |
某烃结构式如下: -C≡C-CH=CH-CH3,有关其结构说法正确的是()
-C≡C-CH=CH-CH3,有关其结构说法正确的是()
| A.所有原子可能在同一平面上 | B.所有原子可能在同一条直线上 |
| C.所有碳原子可能在同一平面上 | D.所有氢原子可能在同一平面上 |
把过量的CO2气体通入下列物质的饱和溶液中,不变浑浊的是()
| A.Ca(OH)2 | B.C6H5ONa | C.NaAlO2 | D.Na2SiO3 |
下列有机物中,一氯取代物种数最多的是()
A.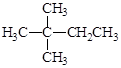 |
B.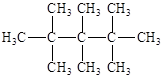 |
C.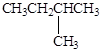 |
D.CH3- -CH3 -CH3 |