某酸性工业废水中含有K2Cr2O7。光照下,草酸H2C2O4能将其中的Cr2O72—转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始c(H+)和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
| 实验编号 |
初始c(H+) |
废水样品体积/mL |
草酸溶液体积/mL |
蒸馏水体积/mL |
| ① |
1.0×10—4 |
60 |
10 |
30 |
| ② |
1.0×10—5 |
60 |
10 |
30 |
| ③ |
1.0×10—5 |
60 |
|
|
测得实验①和②溶液中的Cr2O72—浓度随时间变化关系如图所示。

(2)上述反应后草酸被氧化为 (填化学式)。
(3)实验①和②的结果表明 ;
实验①中0~t1时间段反应速率 (Cr3+)= mol·L—1·min—1 (用代数式表示)。
(Cr3+)= mol·L—1·min—1 (用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一: 起催化作用;假设二: ;假设三: ;
起催化作用;假设二: ;假设三: ;
(5)请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。溶液中Cr2O72—的浓度可用仪器测定)
| 实验方案(不要求写具体操作过程) |
预期实验结果和结论 |
| |
|
“化学多米诺实验”是利用化学反应中气体产生的压力,使多个化学反应依次发生。下图所示就是一个“化学多米诺实验”,其中A~F装置中分别盛放的物质为:
| A.稀硫酸; | B.锌粒; |
| C.某溶液; | D.CaCO3固体;E、滴有紫色石蕊试液的蒸馏水;F、足量的澄清石灰水 |
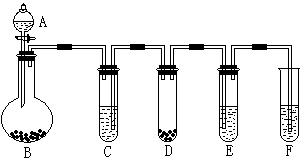
请回答下列问题:
⑴反应开始后,若E中出现红色,F中有白色沉淀生成,则C中的物质可能是
⑵写出装置D中反应的离子方程式:该反应的类型是:
装置F中反应的离子方程式:
⑶上图所示的B~F装置中,发生了氧化还原反应的是
(填装置编号)。请用单线桥表示出电子的转移
某实验需要80 mL、1 mol/L的Na2CO3溶液,现通过如下操作配制:
① 称量g Na2CO3固体放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用玻璃棒搅拌
②待溶液冷却到室温后,小心转入(填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用(填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④将容量瓶塞紧,充分摇匀。
⑤用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都转入容量瓶,并轻轻摇匀
(1)操作步骤正确的顺序是(填序号)。
(2)使用容量瓶前必须进行的一项操作是
(3)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为。
(4)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.1" mol/L的溶液,则稀释后溶液的体积为mL
(5)在配制Na2CO3溶液时,下列操作中的会导致结果偏低
①用拖盘天平称量时砝码放在左盘
②将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
③定容时俯视刻度线
④未冷却到室温就转移到容量瓶中
⑤干净的容量瓶未经干燥就用于配制溶液
(6分) 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
⑴ 图中有两处明显的错误是:①;
②。
⑵ A仪器的名称是,B仪器的名称是。
⑶ 实验时A中除加入少量自来水外,还需要加入少量的,其作用是。
(12分)苯与液溴制取溴苯
(1)制取溴苯的化学反应方程式:
(2)装置A的名称是:
(3)冷凝管作用:冷凝水顺序:(A.上进下出 B.下进上出)
(4)B装置导管位置为什么要处于如图所示位置,而不能伸入液面以下,请解释原因:
(5)实验结束后,得到粗溴苯要用如下操作提纯,①蒸馏;②水洗;③用干燥剂干燥;④用10% NaOH溶液洗;⑤分液。正确的操作顺序是
A.⑤④②①③ B.④②⑤③①
C.④②⑤①③ D.④⑤③①②
(6分)某研究性学习小组成员分别设计了如下甲、乙、丙三套实验装置制取乙酸乙酯。请回答下列问题: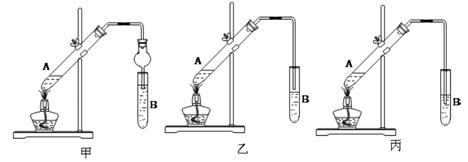
(1)A试管中的液态物质有_______。
(2)甲、乙、丙三套装置中,不宜选用的装置是_______。(选填“甲”、“乙’’、“丙’’)
(3)试管B中的液体能和生成物中混有的杂质发生反应,其化学方程式是_______。