在100 mL含等物质的量的HBr和H2SO3的溶液中通入0.025 mol Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3)。则原溶液中HBr和H2SO3的浓度都等于
| A.0.16 mol·L-1 | B.0.02 mol·L-1 | C.0.20 mol·L-1 | D.0.25 mol·L-1 |
能通过化学反应使溴水褪色,又能使酸性高锰酸钾溶液褪色的是
| A.苯 | B.乙烷 | C.甲烷 | D.乙烯 |
已知N2(g)+3H2(g) 2NH3(g)(正反应放热)。若在高温、高压和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法正确的是
2NH3(g)(正反应放热)。若在高温、高压和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法正确的是
| A.若降低温度,可以加快反应速率 |
| B.使用催化剂是为了加快反应速率 |
| C.在上述条件下,N2的转化率能达到100﹪ |
| D.达到平衡时,N2 、H2和NH3的浓度一定相等 |
下列几种物质均能使品红褪色,其中有一种物质使品红褪色的原理与其他几种不同,该物质是
| A.二氧化硫 | B.次氯酸钙 | C.次氯酸 | D.次氯酸钠 |
下列物质属于同分异构体的一组是
| A.甲烷和乙烷 |
| B.CH4与CH3-CH2-CH3 |
C.CH3-CH2-CH2-CH3 与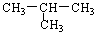 |
| D.苯与环己烷 |
下列反应属于吸热反应的是
| A.生石灰与水的反应 | B.乙醇燃烧 |
| C.铝粉与氧化铁粉末反应 | D.BA(OH)2·8H2O与NH4Cl的反应 |