在不同温度下,向2L密闭容器中加入1molNO和1mol活性炭,发生反应: 2NO(g)+C(g) N2(g)+CO2(g)△H="-213.5kJ" mol-1,达到平衡时的数据如下:
N2(g)+CO2(g)△H="-213.5kJ" mol-1,达到平衡时的数据如下:
| 温度/℃ |
n(活性炭)/mol |
n(CO2)/mol |
| T1 |
0.70 |
|
| T2 |
|
0.25 |
下列说法不正确的是
A.上述信息可推知:T1<T2
B.T1℃时,该反应的平衡常数K=9/16
C.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减
D.T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)不变
盐酸乙哌立松片是一种骨骼肌松弛剂,能改善由肩周炎、腰痛症等引起的肌紧张状况,其结构筒式如下:关于盐酸乙哌立 松片有下列说法:()
松片有下列说法:()
①是芳香族化合物
②含有N原子的六元环上所有原子均处于同一平面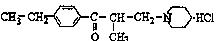
③能发生还原反应
④是一种有机盐。其中正确的是
| A.①③④ | B.①②③ | C.①②④ | D.②③④ |
关于下列各装置图的叙述中,正确的是()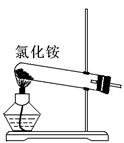
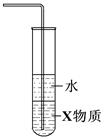

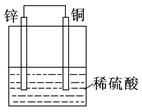
①②③④
| A.实验室用装置①制取氨气 |
| B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| C.装置③可用于制备氢氧化亚铁并观察其颜色 |
D.装置④是原电池,锌电极为负极,发生 还原反应 还原反应 |
下列说法正确的是()
| A.25℃时NH4Cl溶液的KW大于100℃时NH4Cl溶液的KW |
| B.SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O=SO32-+2I- |
C.加入铝粉能产生氢气的溶液中,可能存在大量的Na+、Ba2+、AlO2-、NO3 - - |
| D.100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
下列各项中表达正确的是()
A.H2O2的电子式: |
B. 的命名:2,2—二甲基—2—乙醇 的命名:2,2—二甲基—2—乙醇 |
| C.常温下,浓度都为0.1mol·Lˉ1的Na2CO3、NaHCO3溶液的pH,前者小于后者 |
D. 为二氯化二硫(S2Cl2)的结构,分子中有极性键、非极性键,是极性分子 为二氯化二硫(S2Cl2)的结构,分子中有极性键、非极性键,是极性分子 |
已知-NH2呈碱性,-CONH2呈中性。分子式均为C7H7O2N的以下有机物,对其性质判断正确的是()



甲乙丙丁
①甲物质既有酸性又有碱性②乙物质只有碱性
③丙物质只有酸性④丁物质既不显酸性又不显碱性
| A.①②③④ | B.①②③ | C.①③④ | D.①②④ |