常温下,浓度均为0.1 mol•L-1的4种钠盐溶液pH如下:
| 溶质 |
Na2CO3 |
NaHCO3 |
NaClO |
NaHSO3 |
| pH |
11.6 |
9.7 |
10.3 |
5.2 |
下列说法中不正确的是
A.四种溶液中,Na2CO3溶液中水的电离程度最大
B.向氯水中加入NaHCO3(s),可以增大氯水中次氯酸的浓度
C.NaHSO3溶液显酸性的原因是:NaHSO3=Na++H++SO32-
D.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3
元素A的阳离子aAm+与元素B的阴离子bBn—具有相同的电子层结构。以下关于A.B元素性质的比较中,正确的是()
①原子序数:a>b②离子半径:aAm+<bBn—③原子半径:A<B④元素所在的周期数:A>B⑤A的最高正价与B的最低负价的绝对值相等⑥b = a+m-n
A.②③④ B.①②④ C.④⑤⑥ D.②⑤⑥
下列分子中所有原子都满足最外层8电子结构的是()
① CO2, ② NO2, ③ PCl3, ④ PCl5,
⑤ BeCl2, ⑥ N2
| A.①④⑤ | B.①③⑥ | C.②④ | D.②③④⑤ |
据报道,科学家已成功合成了少量的O4,有关O4的说法正确的是()
| A.O4的摩尔质量是64 g |
| B.O4与O2互为同位素 |
| C.相同质量的O4与O3所含原子个数之比为1∶1 |
| D.O4与O3.O2都是氧元素的同分异构体 |
在一定条件下,恒容的密闭容器中发生如下反应:2SO2(g)+O2(g) 2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能出现的数据是
2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能出现的数据是
| A.C(SO3)=0.4mol·L-1 | B.C(SO3)+C(SO2)=0.15 mol·L-1 |
| C.C(O2)=0.3mol·L-1 | D.C(SO3)+C(SO2)=0.4 mol·L-1 |
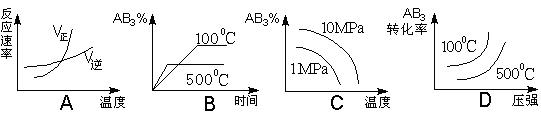
对于可逆反应2AB3(g) 2A(g) + 3B2(g)ΔH>0下列图象不正确的是
2A(g) + 3B2(g)ΔH>0下列图象不正确的是