有等体积、等pH的H2SO4、HCl和CH3COOH三种酸溶液,滴加等浓度的氢氧化钠溶液将它们恰好中和,用去碱的体积分别为V1、V2、V3,则这三者的关系是
| A.V1=V2>V3 | B.V1=V2=V3 | C.V3>V2>V1 | D.V3>V2=V1 |
下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是
| A.CH3CH2CH3 | B.CH3COCH2CH2CH3 | C.CH3CH2OH | D.CH3OCH3 |
在恒温、恒容的条件下,有反应2A(g)+2B(g)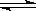 C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2 mol/L和6mol/L。则以下叙述正确的是
C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2 mol/L和6mol/L。则以下叙述正确的是
A.两途径最终达到平衡时,体系内混合气的压强相同
B.两途径最终达到平衡时,体系内混合气的百分组成不同
C.达平衡时,途径Ⅰ的反应速率v(A)等于途径Ⅱ的反应速率v(A)
D.达平衡时,途径Ⅰ所得混合气的密度为途径Ⅱ所得混合气密度的1/2
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见右图,电池总反应可表示为:2H2+O2 ="==" 2H2O下列有关说法正确的是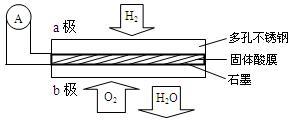
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e-="==" 4OH- |
| C.每转移0.1 mol电子,消耗1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
下列说法正确的是
| A.pH = 3的盐酸和pH = 5的硫酸等体积混合,pH = 4 |
| B.室温下,pH = 9的碱性溶液中,可能存在CH3COOH分子 |
| C.中性溶液中必然有c(H+) = c(OH-) = 1×10-7 mol/L |
| D.在0.1 mol/L HCl溶液中加入适量的蒸馏水,溶液中各种离子的物质的量浓度均减小 |
用来表示可逆反应:2A(g)+B(g)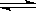 3C(g)(正反应放热)的正确图象是下图中的
3C(g)(正反应放热)的正确图象是下图中的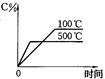

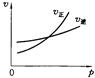

A B C D