在一定条件下,向一带活塞的密闭容器中充入2mol NO2,发生下列反应2NO2(g)⇌N2O4(g) ΔH < 0,达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图。下列对t1时刻改变条件的推测中正确的是
| A.保持容器体积不变,升高反应温度 |
| B.保持温度和容器体积不变,充入1mol N2(g) |
| C.保持温度和容器体积不变,充入1mol N2O4(g) |
| D.保持温度和压强不变,充入1mol N2O4(g) |
下列关于乙烯和乙烷的说法中,不正确的是
| A.乙烯属于不饱和链烃,乙烷属于饱和链烃 |
| B.乙烯分子中所有原子处于同一平面上,乙烷分子中的原子不在同一平面上 |
C.乙烯分子中的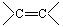 双键比乙烷分子中的C—C单键更稳定,性质更活泼 双键比乙烷分子中的C—C单键更稳定,性质更活泼 |
| D.乙烯能使酸性KMnO4溶液褪色,乙烷不能 |
下列关于有机化合物的说法正确的是
| A.乙醇和乙酸都存在碳氧双键 |
| B.甲烷和乙烯都可以与氯气反应 |
| C.高锰酸钾可以氧化苯和甲烷 |
| D.乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
可以用分液漏斗分离的一组液体混合物是
| A.溴和四氯化碳 | B.苯和溴苯 |
| C.水和硝基苯 | D.苯和汽油 |
下列各组物质中,一定既不是同系物,又不是同分异构体的是
A.CH4和C4H10 B.乙酸和甲酸甲酯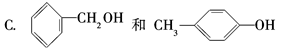 D.苯甲酸和
D.苯甲酸和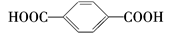
下列有机化合物的分类不正确的是
| A |
B |
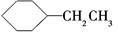 |
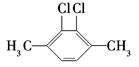 |
| 苯的同系物 |
芳香族化合物 |
| C |
D |
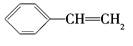 |
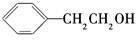 |
| 不饱和烃 |
醇 |