某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验: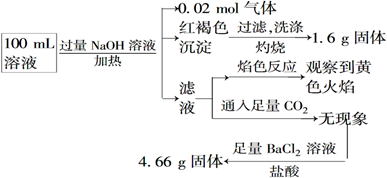
下列说法正确的是
| A.原溶液中c(Fe3+)=0.2 mol·L-1 |
| B.要确定原溶液中是否含有Fe2+,其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+ |
| C.SO42-、NH4+、Na+一定存在,CO32-,Al3+一定不存在 |
| D.溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol·L-1 |
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是()
| A.称量 | B.溶解 | C.转移 | D.定容 |
下列实验误差分析错误的是()
| A.用湿润的pH试纸测稀碱液的pH,测定值偏小 |
| B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小 |
| D.测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小 |
下列操作不能达到目的的是()
| 选项 |
目的 |
操作 |
| A. |
配制100 mL 1.0 mol/L CuSO4溶液 |
将25 g CuSO4·5H20溶于100 mL蒸馏水中 |
| B. |
除去KNO3中少量NaCl |
将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C. |
在溶液中将MnO4-完全转化为Mn2+ |
向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 |
| D. |
确定NaCl溶液中是否混有Na2CO3 |
取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
下列实验中,所采取的分离方法与对应原理都正确的是()
| 选项 |
目的 |
分离方法 |
原理 |
| A. |
分离溶于水中的碘 |
乙醇萃取 |
碘在乙醇中的溶解度较大 |
| B. |
分离乙酸乙酯和乙醇 |
分液 |
乙酸乙酯和乙醇的密度不同 |
| C. |
除去KNO3固体中混杂的NaCl |
重结晶 |
NaCl在水中的溶解度很大 |
| D. |
除去丁醇中的乙醚 |
蒸馏 |
丁醇与乙醚的沸点相差较大 |
用右图所示装置检验乙烯时不需要除杂的是