反应N2O4(g) 2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是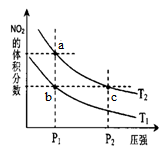
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a浅,c深 |
| C.a、b两点气体的平均相对分子质量:a>b |
| D.b、c两点化学平衡常数:b<c |
下列关于高分子化合物的组成、结构、性质的说法正确的是
| A.高分子化合物的相对分子质量都很大 |
| B.纯净的淀粉属于纯净物 |
| C.线型高分子具有热固性 |
| D.高分子材料都不易燃烧 |
食品香精菠萝酯的生产路线(反应条件略去)如下:
下列叙述正确的是
| A.步骤(1)、(2)的反应类型不同 |
| B.步骤(1)产物中残留的苯酚可用FeCl3溶液检验 |
| C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 |
| D.步骤(2)产物中残留的烯丙醇可用溴水检验 |
下列有关实验装置及用途叙述正确的是

| A.a装置检验消去产物,中间应加水洗装置 |
| B.b装置检验酸性:盐酸>碳酸>苯酚 |
| C.c装置用于实验室制取并收集乙烯 |
| D.d装置用于实验室制硝基苯 |
下列根据事实所作出的结论正确的是
| 事实 |
结论 |
| A.甲乙两种物质,相对分子质量相同,结构不同 |
甲和乙一定是同分异构体 |
| B.灼烧棉织品、羊毛衫和涤纶衣物 |
有烧焦羽毛气味的是羊毛衫 |
| C.在淀粉溶液中加入市售的加碘食盐不出现蓝色 |
不能说明此盐不含碘元素 |
| D.完全燃烧产物是CO2和H2O的物质 |
一定只含C、H元素 |
下列说法正确的是
| A.2—丁醇发生消去反应产物有2 种 |
| B.卤代烃都能发生水解反应 |
| C.醇在Cu/△条件下都能氧化成醛 |
D. 在酸性条件下水解产物是 在酸性条件下水解产物是 和C2H5OH 和C2H5OH |