已知某溶液中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:
①取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;②将沉淀过滤、洗涤、灼烧,得到1.6 g固体;
③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。
请回答下列问题:
(1)结合①和②,判断原溶液中肯定含有的离子是 ,可以排除的离子是 。
(2)由③推知原溶液中一定有 离子,其物质的量为 mol。
(3)综合(1)、(2)及题干信息,结合溶液中电荷守恒知识,还可以排除的离子是 。该学习小组最终得出结论:该溶液由 种阳离子(填数字,下同)和 种阴离子组成。
由乙烯和其他无机原料合成环状酯,其合成过程如下(水及其他无机产物均已省略)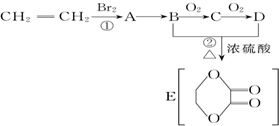
请分析后回答下列问题:
(1)写出下列反应的反应类型:①______________;②______________;
(2)D物质中的官能团名称为______________;
(3)物质X与A互为同分异构体,则X的结构简式为______________;
(4)写出下列转化的化学方程式:A→B______________;
B+D→______________。
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X的原子结构示意图为________________ Y原子核外价电子排布图 ________________。
(2)XZ2与YZ2分子的立体结构分别是________和________________,相同条件下两者在水中的溶解度较大的是__________(写分子式),理由是_________________________。
(3)Q的元素符号是__________,它的基态原子的核外电子排布式为______________,在形成化合物时它的最高化合价为__________。
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键_____________________。
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738 kJ·mol-1 I2=1451 kJ·mol-1 I3=7733 kJ·mol-1 I4=10540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:______________________________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有__________个方向,原子轨道呈_______形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背___________________。
该同学所画的电子排布图违背___________________。
(4)G位于________族________区,该元素的核外电子排布式为_________________。
(5)DE3中心原子的杂化方式为____________,用价层电子对互斥理论推测其空间构型为__________。
(6)检验F元素的方法是____________,请用原子结构的知识解释产生此现象的原因:_____________。
已知甲、乙、丙为常见单质,A、B、C、D、E、F、G、H均为常见的化合物;B和乙为淡黄色固体,E的式量比D的式量大16,在一定条件下,各物质间相互转化关系如下图所示(产物中水已忽略)。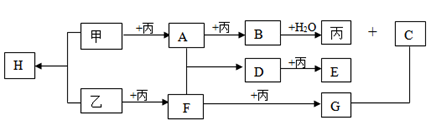
(1)写出下列物质的化学式:丙_______、B_______、D_______。
(2)写出有关反应的化学方程式:
B+H2O _______________________________________
D + 丙 ______________________________________
F+ 丙 _______________________________________
(1)下图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀。
①根据如图转化关系,填写下列物质的化学式:A为______D为______E为______
②写出B→C的化学方程式_________________________
③写出B→A的化学方程式_________________________
(2)把某黑色固体单质A加热至红热,投入到一种无色溶液B中,产生由两种气体组成的混合气体X,将X做如下图所示的实验:
①由此可推断各物质的化学式为:C为___________X为___________
②写出A投入B中的化学方程式______________________
③写出D的稀溶液与F反应的离子方程式__________________