在容积固定的密闭容器中,进行下列反应A(g)+B(g) 2C(?)+D(g),此反应符合下列两个图像(其中φ代表物质的百分含量),则下列判断正确的是( )
2C(?)+D(g),此反应符合下列两个图像(其中φ代表物质的百分含量),则下列判断正确的是( )

| A.物质C不可能为气态 |
| B.正反应为吸热反应 |
| C.该反应,升高温度平衡正向移动 |
| D.300℃下该反应到达平衡状态后,迅速充入He,平衡正向移动 |
下列行为不符合“绿色化学”这一主题的是
| A.推广和鼓励多使用公共交通工具出行 |
| B.大量使用化肥农药,提高农作物产量 |
| C.大力发展太阳能和风力发电 |
| D.对燃煤进行脱硫,减少空气的污染 |
某溶液中可能含有下列5种离子中的几种:Na+、NH4+、Mg2+、Al3+、Cl-。为确认该溶液组成进行如下实验:①取20.0 mL该溶液,加入32.5 mL 4.00 mol•L-1 NaOH溶液加热,有白色沉淀产生,无刺激气味气体生成.过滤、洗涤、干燥,得沉淀2.03 g。再将滤液稀释至100mL,测得滤液中c(OH-)="0.2" mol•L-1;②另取20.0 mL该溶液,加入足量的AgNO3溶液,生成白色沉淀14.35 g。关于原溶液组成结论正确的是
| A.一定含有Mg2+、Al3+、Cl-,不含有Na+、NH4+ |
| B.一定含有Na+、Mg2+、Cl-,不含有NH4+、可能含有Al3+ |
| C.c(Mg2+)为1.75 mol•L-1,c(Na+)为1.50 mol•L-1 |
| D.c(Cl-)为5.00 mol•L-1,c(Al3+)为1.00 mol•L-1 |
短周期元素A、B、C、D、E,原子序数依次增大。已知元素A的气态氢化物和A的最高价氧化物对应的水化物反应生成盐;B、E为同主族元素,B元素原子最外层电子数是次外层的3倍;D是地壳中含量最多的金属元素;C是短周期中与水反应最激烈的金属元素。下列叙述不正确的是
A.元素A的氧化物常温下一般均为无色无味气体
B.元素C、D、E的最高价氧化物对应的水化物两两之间能发生反应
C.原子半径:C>D>B
D.元素B的气态氢化物的沸点比元素E气态氢化物的沸点高
下列反应属于加成反应的是
A.CH4+Cl2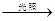 CH3Cl+HCl CH3Cl+HCl |
B.CH2=CH2 + HCl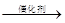 CH3CH2Cl CH3CH2Cl |
C.2CH3CH2OH + O2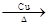 2CH3CHO+2H2O 2CH3CHO+2H2O |
D.2C6H6 + 15O2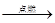 12CO2 +6H2O 12CO2 +6H2O |
下列关于Na2CO3和NaHCO3的说法中不正确的是
| A.可用澄清石灰水鉴别这两种物质 |
| B.Na2CO3比NaHCO3更稳定 |
| C.相同条件下0.5 mol/L Na2CO3溶液碱性比NaHCO3强 |
| D.等物质的量的Na2CO3和NaHCO3与足量盐酸反应生成的二氧化碳质量相等 |