关于下列图示的说法中正确的是:
| A.图①装置用于分离沸点相关较大的互溶液体混合物 |
| B.图②装置用于研究不同催化剂对反应速率的影响 |
| C.图③中电流计的指针发生偏转,石墨为正极 |
| D.图④装置可用于检验溴乙烷与NaOH的醇溶液共热产生的乙烯 |
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.60 mL | B.45 mL | C.30 mL | D.15 mL |
某溶液中含有HCO3-、CO32-、SO32-、Na+、NO3-五种离子,若向其中加入Na2O2粉末充分反应后(溶液体积变化忽略不计),溶液中离子浓度保持不变的是
| A.NO3- | B.CO32-、NO3- |
| C.SO32-、NO3- | D.CO32-、NO3-、Na+ |
四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2 和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为
| A.①>②>③>④ | B.①=②=③=④ |
| C.①=②=③>④ | D.①=②>③>④ |
下列实验现象所对应的离子方程式不正确的是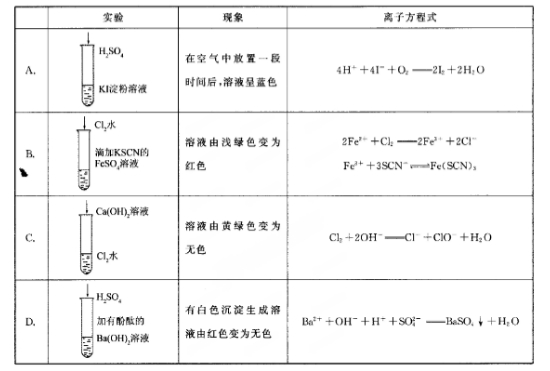
常温下,下列各组离子在指定溶液中一定能大量共存的是