一定条件下合成乙烯:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是:
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是:
| A.生成乙烯的速率:v(M)有可能小于v(N) |
| B.平衡常数:KM>KN |
| C.当温度高于250℃,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低 |
| D.若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7% |
工业用CaO和硝酸反应制Ca(NO3)2·4H2O晶体,为确保制备过程既不补充水分,又无水剩余,则应选用的硝酸质量分数()
| A.30% | B.63% | C.70% | D.84% |
关于下列各装置图的叙述中,不正确的是()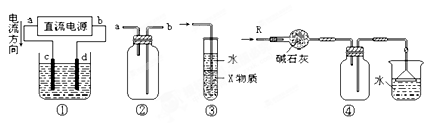
| A.装置①中,d为阴极、c为阳极 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、N2、、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,(NH3和HCl不溶于CCl4)并可防止倒吸 |
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li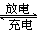 LiFePO4,含Li+ 的导电固体为电解质。下列有关LiFePO4电池说法正确的是()
LiFePO4,含Li+ 的导电固体为电解质。下列有关LiFePO4电池说法正确的是()
| A.可加入硫酸以提高电解质的导电性 |
| B.充电过程中,阳极LiFePO4的质量减少 |
| C.放电时电池内部Li+ 向负极移动 |
| D.放电时电池负极反应为:FePO4+Li++e-= LiFePO4 |
某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥C032-⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示。则该溶液中一定含有的离子是()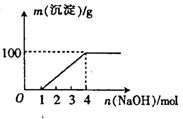
| A.②⑤⑥⑦ |
| B.②③⑤⑦ |
| C.①②③⑥⑦ |
| D.①②③④⑤⑦ |
现有X、Y、Z、W四种短周期元素,原子半径:r(X)>r(Y)>r(Z)>r(W)。X、Y、Z处于同一周期,Z、W处于同一主族;X、Y、Z的原子序数之和为40。下列说法中正确的是()
| A.Y的最高价氧化物对应的水化物一定是强碱 |
| B.Z一定位于第三周期ⅦA族 |
| C.若X、Y、W可形成化合物XYW2,则该化合物的水溶液呈碱性 |
| D.X与足量的W加热反应会生成化合物X2W |